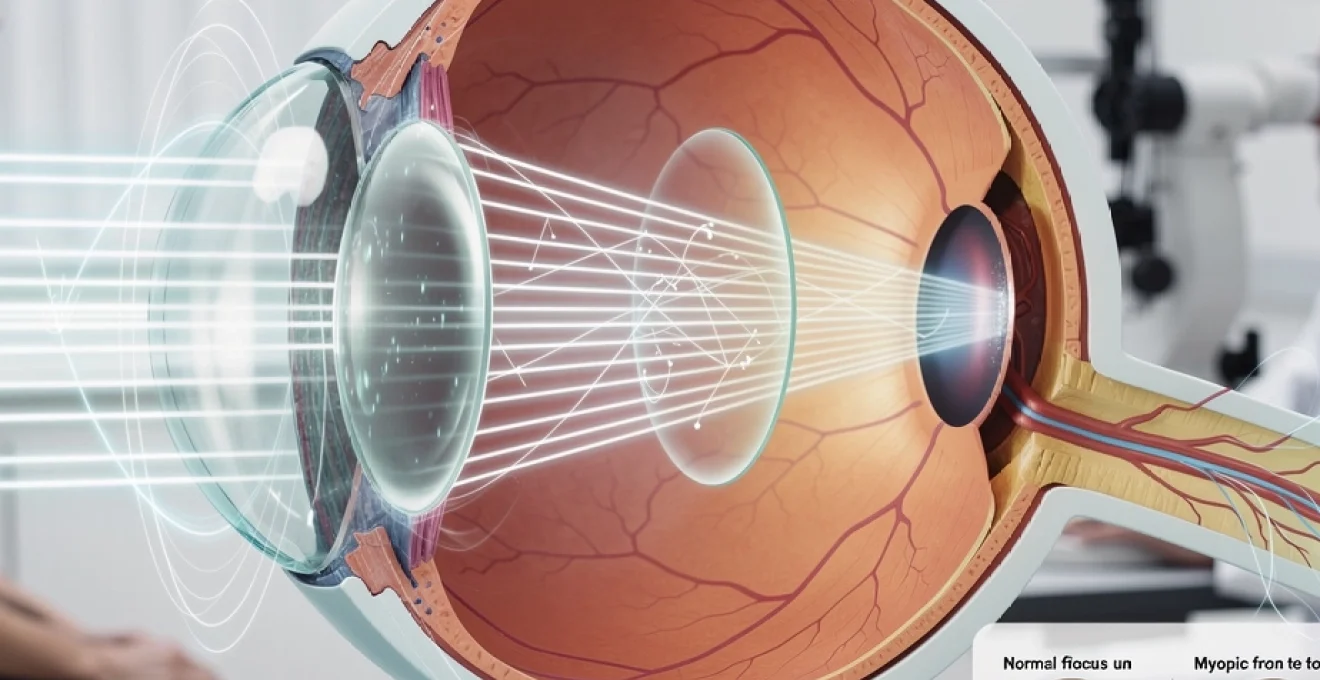
La vision humaine repose sur un mécanisme optique d’une précision remarquable, où chaque élément anatomique joue un rôle crucial dans la déviation et la focalisation des rayons lumineux. L’œil fonctionne comme un système optique complexe, capable de transformer les ondes électromagnétiques en images nettes grâce à une succession de structures réfractives spécialisées. Cette transformation implique des phénomènes physiques sophistiqués régis par les lois de l’optique géométrique, notamment la loi de Snell-Descartes, qui gouvernent le comportement de la lumière lors de son passage d’un milieu à un autre. Comprendre ces mécanismes permet d’appréhender non seulement le fonctionnement normal de la vision, mais aussi les anomalies réfractives et leurs corrections modernes.
Anatomie structurelle de l’appareil oculaire et ses éléments réfractifs
L’architecture oculaire présente une organisation remarquable où cinq milieux transparents participent successivement à la réfraction lumineuse. Cette succession de structures aux propriétés optiques distinctes permet une focalisation progressive et optimale des rayons sur la rétine. Chaque élément possède un indice de réfraction spécifique, caractéristique fondamentale qui détermine sa capacité à dévier la lumière selon un angle précis.
Architecture de la cornée et son indice de réfraction de 1,376
La cornée constitue le premier et principal élément réfractif du système visuel, avec un pouvoir dioptrique représentant environ 65% de la puissance totale de l’œil. Sa structure multicouche comprend l’épithélium antérieur, la membrane de Bowman, le stroma cornéen, la membrane de Descemet et l’endothélium postérieur. L’indice de réfraction cornéen de 1,376 crée un gradient optique significatif avec l’air ambiant (n=1,000), générant ainsi la déviation lumineuse la plus importante du trajet optique. Cette différence d’indice explique pourquoi la cornée contribue massivement à la convergence des rayons incidents, bien que sa courbure soit moins prononcée que celle du cristallin.
Composition biochimique de l’humeur aqueuse et sa densité optique
L’humeur aqueuse, avec son indice de réfraction de 1,336, remplit les chambres antérieure et postérieure du segment antérieur oculaire. Sa composition, proche du plasma sanguin mais dépourvue de protéines, lui confère une transparence parfaite essentielle à la transmission lumineuse. Cette substance liquide maintient la pression intraoculaire tout en assurant le métabolisme des structures avasculaires environnantes. Son renouvellement constant, effectué par le corps ciliaire selon un cycle de 90 minutes environ, garantit la stabilité de ses propriétés optiques. La différence d’indice entre la cornée et l’humeur aqueuse (Δn = 0,040) modifie légèrement la trajectoire des rayons à l’interface cornéo-aqueuse.
Structure lamellaire du cristallin et gradient d’indice protéique
Le cristallin présente une architecture lamellaire unique où l’indice de réfraction varie de manière centripète, passant de 1,386 en périphérie à 1,406 au centre du noyau cristallinien. Cette variation d’indice, appelée gradient d’indice, résulte de la concentration progressive des protéines cristalliniennes (cristallines α, β et γ) vers le centre de la lentille. Ce gradient permet
de mieux contrôler la focalisation des rayons lumineux et de limiter certaines aberrations optiques internes. Sur le plan mécanique, le cristallin est avasculaire, encapsulé dans une fine capsule basale élastique, et suspendu par les fibres zonulaires au muscle ciliaire. Sa transparence dépend de l’agencement extrêmement régulier des fibres cristalliniennes et de l’absence quasi totale d’organites intracellulaires dans la zone centrale, ce qui réduit la diffusion de la lumière. Avec l’âge, la compaction des fibres et la modification du gradient d’indice entraînent une perte de souplesse et une augmentation de la densité, participant à la fois à la presbytie et au risque de cataracte nucléaire.
Propriétés optiques du corps vitré et transmission lumineuse
Le corps vitré occupe près de 80% du volume intraoculaire et présente un indice de réfraction d’environ 1,336, comparable à celui de l’humeur aqueuse. Il s’agit d’un gel transparent composé majoritairement d’eau (plus de 98%), structuré par un réseau de fibres de collagène et des molécules d’acide hyaluronique. Sa fonction optique principale est d’assurer une transmission lumineuse quasi sans diffusion vers la rétine, tout en maintenant la forme du globe et l’apposition de la rétine sensorielle sur l’épithélium pigmentaire.
Chez l’adulte jeune, le vitré est homogène et parfaitement transparent, ce qui minimise les phénomènes de diffusion de la lumière et de dégradation du contraste rétinien. Avec l’avancée en âge, une liquéfaction progressive (synérèse vitréenne) et des condensations fibreuses peuvent apparaître, se manifestant cliniquement par des « mouches volantes ». Si ces modifications affectent peu la réfraction globale, elles peuvent néanmoins perturber localement la qualité de la transmission lumineuse et engendrer des ombres mobiles projetées sur la rétine. Dans les situations extrêmes (décollement postérieur du vitré ou hémorragie vitréenne), la diffusion ou l’absorption de la lumière peut devenir suffisamment importante pour compromettre la netteté de l’image rétinienne.
Mécanismes de réfraction cornéenne et aberrations chromatiques
La réfraction cornéenne représente la première grande étape de déviation des rayons lumineux dans l’œil. C’est à ce niveau que s’exprime de façon la plus marquée la loi de Snell-Descartes, en raison du brusque changement d’indice entre l’air et le tissu cornéen. Mais la cornée n’est pas un simple dioptre sphérique idéal : sa géométrie réelle, ses micro-irregularités et sa nature dispersive induisent des aberrations optiques, dont certaines sont bénéfiques, d’autres délétères pour la qualité de vision. Comprendre ces phénomènes permet de mieux appréhender pourquoi deux yeux ayant la même acuité sur une charte peuvent offrir des qualités de vision très différentes, notamment en basse lumière ou en présence de halos.
Loi de Snell-Descartes appliquée à l’interface air-cornée
À l’interface air-cornée, la lumière subit une déviation dictée par la loi de Snell-Descartes : n₁·sin(i) = n₂·sin(r), où n₁ est l’indice de l’air (≈1,000), n₂ celui de la cornée (≈1,376), i l’angle d’incidence et r l’angle de réfraction. Cette discontinuité d’indice très marquée fait de la face antérieure de la cornée le dioptre le plus puissant de l’ensemble du système optique oculaire. Plus l’angle d’incidence s’éloigne de la normale à la surface cornéenne, plus la déviation est importante, ce qui explique la sensibilité de la réfraction cornéenne aux modifications de courbure ou aux irrégularités locales.
Dans les conditions physiologiques, les rayons proches de l’axe optique (petits angles) obéissent à une approximation quasi linéaire de la loi des sinus, ce qui simplifie les calculs de réfraction et de vergence. En pratique clinique, on exploite cette loi pour modéliser l’effet de toute modification de la courbure cornéenne (chirurgie réfractive, kératocône, cicatrices) sur la focalisation rétinienne. Il est intéressant de noter qu’un simple changement de rayon de courbure de quelques dixièmes de millimètre suffit à modifier la réfraction oculaire de plusieurs dioptries, illustrant à quel point l’interface air-cornée est optiquement déterminante.
Puissance dioptrique cornéenne moyenne de 43 dioptries
La cornée possède une puissance dioptrique moyenne d’environ +43 dioptries, sur un total d’environ +60 dioptries pour l’œil emmétrope. Concrètement, cela signifie qu’à elle seule, la cornée est capable de faire converger des rayons parallèles (provenant de l’infini optique) vers un foyer situé à une vingtaine de millimètres en arrière, à proximité de la rétine. Cette forte puissance est essentiellement liée à la courbure de la face antérieure cornéenne, dont le rayon moyen avoisine 7,8 mm.
En pratique, la puissance cornéenne n’est pas parfaitement constante d’un individu à l’autre : elle varie typiquement entre 40 et 48 dioptries, ce qui contribue aux différences de réfraction (myopie ou hypermétropie) indépendamment de la longueur axiale de l’œil. Les appareils modernes de topographie cornéenne et de biométrie optique mesurent précisément cette puissance pour calculer la correction optique idéale (lunettes, lentilles, implants intraoculaires). Pour vous donner un ordre d’idée, une variation de seulement 1 dioptrie de puissance cornéenne peut suffire à passer d’une vision nette sans correction à un flou notable de loin.
Astigmatisme cornéen naturel et irrégularités topographiques
Contrairement à une lentille parfaitement sphérique, la cornée présente le plus souvent une surface toroïdale : sa courbure n’est pas identique dans tous les méridiens. Cette asymétrie entraîne un astigmatisme cornéen physiologique, généralement faible (inférieur à 1 dioptrie) mais quasi universel. Dans l’astigmatisme régulier, deux méridiens principaux, perpendiculaires l’un à l’autre, présentent des courbures différentes, ce qui fait que les rayons lumineux se focalisent en deux lignes focales plutôt qu’en un point unique sur la rétine.
Les topographes cornéens modernes permettent de visualiser la carte de courbure cornéenne comme une « carte de relief », mettant en évidence ces variations de puissance selon les méridiens. Lorsque ces irrégularités deviennent marquées ou anarchiques (kératocône, déformations postopératoires, cicatrices), on parle d’astigmatisme irrégulier. Dans ce cas, la focalisation des rayons se disperse en multiples foyers, dégradant fortement la qualité d’image et générant des phénomènes de flou, de dédoublement ou de halos. Vous avez peut-être remarqué que certaines personnes se plaignent de « voir les lettres déformées ou étirées » : c’est souvent l’expression subjective d’un astigmatisme cornéen significatif.
Aberrations sphériques cornéennes et coefficient de zernike
Même en l’absence d’astigmatisme, une cornée parfaitement régulière mais non parfaitement sphérique engendre des aberrations sphériques. Celles-ci correspondent au fait que les rayons périphériques sont focalisés à une distance différente des rayons paraxiaux (proches de l’axe). En d’autres termes, la cornée ne focalise pas tous les rayons au même point, ce qui a pour effet de réduire le contraste et la netteté de l’image rétinienne, surtout lorsque la pupille est dilatée (vision nocturne, mydriase médicamenteuse).
Pour quantifier ces aberrations de haut degré, l’aberrométrie oculaire utilise une décomposition mathématique en polynômes de Zernike. L’aberration sphérique est décrite par un coefficient spécifique (souvent noté Z₄⁰) dont la valeur permet d’évaluer l’impact de la cornée (et du cristallin) sur la qualité d’optique globale. En pratique, certaines aberrations sphériques modérées peuvent améliorer la profondeur de champ (un peu comme un objectif photo légèrement « sous-corrigé »), au prix d’une légère baisse de contraste. À l’inverse, des aberrations sphériques élevées, par exemple après certaines chirurgies réfractives anciennes ou en cas de cornée très bombée, peuvent induire une vision très dégradée, avec halos autour des sources lumineuses et gêne marquée la nuit.
Accommodation cristallinienne et modulation de la vergence oculaire
Si la cornée fournit la majeure partie de la puissance optique de l’œil, le cristallin en est le régulateur dynamique. Grâce à l’accommodation, l’œil humain est capable d’ajuster en continu sa vergence pour maintenir une image nette sur la rétine, quelle que soit — dans certaines limites — la distance de l’objet observé. Ce mécanisme repose sur une interaction fine entre la capsule cristallinienne, les fibres zonulaires et le muscle ciliaire. Avec le temps, l’efficacité de ce système diminue, conduisant à la presbytie et à la nécessité de porter des lunettes de près.
Mécanisme de helmholtz et contraction du muscle ciliaire
Le mécanisme accommodatif le plus largement admis est celui décrit par Helmholtz au XIXe siècle. Selon ce modèle, en vision de loin, le muscle ciliaire est relâché, ce qui tend fortement les fibres zonulaires attachées à la capsule cristallinienne. Le cristallin est alors étiré et aplati, présentant une puissance réfractive plus faible adaptée aux objets éloignés. Lorsque nous portons notre regard sur un objet proche, le muscle ciliaire se contracte, réduisant le diamètre de l’anneau ciliaire et relâchant la tension zonulaire : le cristallin, libéré, reprend une forme plus sphérique sous l’effet de son élasticité propre, augmentant sa puissance.
Ce changement de courbure est particulièrement marqué sur la face antérieure du cristallin, qui bombe vers l’avant, alors que la face postérieure se modifie plus modestement. L’accommodation s’accompagne souvent d’un myosis (rétrécissement pupillaire) et d’une convergence des deux yeux : ce trio forme la triade accommodative. À l’échelle du quotidien, c’est ce mécanisme qui nous permet de passer de la lecture de notre téléphone à la vision de la route sans effort conscient. Vous avez l’impression que vos yeux « travaillent » plus en fin de journée sur l’ordinateur ? C’est souvent le signe d’une sollicitation accommodative soutenue, surtout si la correction optique n’est pas parfaitement adaptée.
Élasticité capsulaire cristallinienne selon fincham
Les travaux de Fincham ont mis en lumière le rôle central de la capsule cristallinienne dans la mécanique accommodative. Cette fine membrane basale joue un rôle de ressort élastique qui, en interaction avec les fibres zonulaires, permet au cristallin de changer de forme. Chez le sujet jeune, la capsule est suffisamment souple pour se déformer rapidement et revenir à son état initial dès que la contraction ciliaire cesse. Cette élasticité capsulaire, associée à la relative plasticité du noyau et du cortex cristalliniens, assure une amplitude accommodative importante.
Avec l’âge, non seulement le noyau cristallinien se densifie, mais la capsule elle-même perd de son élasticité. Les études biomécaniques montrent une réduction progressive de la capacité de la capsule à exercer des forces efficaces sur la masse cristallinienne. De plus, les modifications de la jonction zonule-capsule perturbent la transmission optimale des forces générées par le muscle ciliaire. Résultat : même si le muscle ciliaire reste fonctionnel, le système mécanique qu’il actionne devient progressivement moins réactif, ce qui se traduit cliniquement par une baisse de la capacité de mise au point de près.
Amplitude accommodative et presbytie liée à l’âge
L’amplitude accommodative désigne la différence entre la vergence maximale et minimale que l’œil peut adopter grâce à l’accommodation. Chez l’enfant, cette amplitude peut atteindre 12 à 14 dioptries, permettant de focaliser des objets à quelques centimètres seulement. À partir de la vingtaine, cette réserve commence déjà à diminuer, souvent à notre insu, pour ne devenir gênante qu’aux alentours de 40–45 ans, lorsque l’amplitude résiduelle tombe en dessous de 4 dioptries environ.
La presbytie correspond précisément à cette diminution physiologique de l’amplitude accommodative liée à l’âge. Le point proche recule progressivement, rendant la lecture fine ou le travail rapproché de plus en plus difficiles sans compensation optique. Vous tendez les bras pour lire ou augmentez la taille des caractères sur votre écran ? C’est souvent le premier signe fonctionnel d’une réserve accommodative insuffisante. D’un point de vue optique, la presbytie n’est pas une maladie mais l’expression d’une limitation mécanique croissante du système cristallinien, qui peut être compensée par des verres de lecture, des verres progressifs ou certaines techniques de chirurgie réfractive.
Variation dioptrique cristallinienne de 15 à 20 dioptries
La contribution accommodative du cristallin représente, chez le sujet jeune, une variation de puissance de l’ordre de 15 à 20 dioptries entre la vision de loin et la vision de très près. En position de repos (vision à l’infini), la puissance cristallinienne se situe autour de +19 dioptries, tandis qu’en accommodation maximale, elle peut dépasser +30 dioptries. Cette impressionnante variabilité est rendue possible par la combinaison d’un gradient d’indice interne, d’une capsule élastique et d’un système musculaire finement contrôlé par le système nerveux autonome.
Au fur et à mesure du vieillissement, cette plage de variation se réduit drastiquement, jusqu’à devenir quasi nulle au-delà de 60 ans, où le cristallin se comporte alors comme une lentille presque rigide. Cette perte de flexibilité explique pourquoi certaines solutions chirurgicales modernes tentent de mimer la multifocalité ou la profondeur de champ plutôt que de restaurer l’accommodation véritable. En pratique, comprendre cette variation dioptrique est essentiel pour calculer la puissance des implants intraoculaires dits « accommodatifs » ou « multifocaux », qui cherchent à redonner une partie de cette capacité à voir net à plusieurs distances.
Formation de l’image rétinienne et optimisation de la focalisation
Une fois réfractés par la cornée, l’humeur aqueuse, le cristallin et le vitré, les rayons lumineux doivent converger au plus près de la fovéa, au centre de la macula, pour assurer une vision fine et détaillée. La rétine fonctionne comme un écran sensoriel, mais un écran « intelligent », capable d’analyser, de filtrer et de prétraiter les informations lumineuses avant de les transmettre au cerveau. La netteté de l’image rétinienne dépend de la précision de la focalisation, de la taille de la pupille, des aberrations optiques globales et de l’architecture des photorécepteurs.
Sur le plan purement géométrique, un œil emmétrope focalise les rayons parallèles provenant de l’infini sur le plan rétinien, à environ 22 à 24 mm en arrière de la cornée. Lorsque la focalisation est parfaite, les points de l’objet observé correspondent à des taches minimales sur la rétine, idéalisées par la fonction d’étalement du point (PSF). Plus cette PSF est concentrée, meilleure est la résolution spatiale et le contraste de l’image. L’aberrométrie moderne permet de calculer cette PSF à partir de la mesure du front d’onde traversant l’œil, offrant une représentation quantitative de la qualité optique globale.
L’optimisation de la focalisation ne dépend pas uniquement de l’optique : la taille et la distribution des cônes au niveau de la fovéa jouent un rôle tout aussi crucial. Chaque cône fovéal couvre un angle visuel extrêmement réduit, de l’ordre d’une minute d’arc, ce qui fixe en pratique la limite théorique de résolution de l’œil humain. La profondeur de champ oculaire, quant à elle, est influencée par le diamètre pupillaire : une petite pupille (2–3 mm) augmente la profondeur de champ, tolérant de légères erreurs de focalisation, tandis qu’une grande pupille (6–7 mm) accentue les effets des aberrations et réduit cette tolérance. C’est pour cela que nous voyons souvent plus net en lumière forte qu’au crépuscule, à correction identique.
Pathologies réfractives et anomalies de la focalisation oculaire
Lorsque la longueur de l’œil ou la puissance des éléments réfractifs ne sont plus en adéquation, la focalisation des rayons lumineux ne se fait plus exactement sur la rétine. On parle alors d’amétropies, c’est-à-dire de défauts de réfraction. Ces anomalies ne sont pas des maladies en soi, mais des variantes géométriques du système optique, qui peuvent toutefois altérer sérieusement la qualité de vie si elles ne sont pas corrigées. Comprendre où se forme l’image par rapport à la rétine permet de distinguer les principaux profils réfractifs.
Dans la myopie, l’œil est généralement trop long ou trop puissant : les rayons parallèles se focalisent en avant de la rétine. Le sujet voit bien de près mais mal de loin, et la vision nocturne est souvent particulièrement dégradée du fait de la dilatation pupillaire et des aberrations accrues. À l’inverse, dans l’hypermétropie, l’œil est trop court ou pas assez puissant : l’image nette se situerait en théorie en arrière de la rétine. Le sujet doit alors réaliser un effort accommodatif permanent, même pour voir net de loin, ce qui peut entraîner fatigue visuelle, céphalées ou flou intermittent, surtout chez l’enfant et l’adulte jeune.
L’astigmatisme correspond à une différence de puissance entre deux méridiens principaux de l’œil, le plus souvent liée à la cornée mais parfois au cristallin. Les images sont déformées, étirées ou dédoublées, en particulier sur les lignes et les contrastes marqués. Lorsque s’ajoute une presbytie, la combinaison des défauts peut rendre la lecture et le travail sur écran particulièrement inconfortables sans correction adaptée. Enfin, certaines anomalies plus complexes, comme le kératocône ou les séquelles de chirurgie ou de traumatisme, génèrent des aberrations optiques de haut degré qui ne se résument pas à une simple sphère et un cylindre, et nécessitent des solutions optiques plus sophistiquées (lentilles rigides, implants spéciaux).
Technologies correctrices et chirurgie réfractive moderne
La compréhension fine des mécanismes de réfraction oculaire et des aberrations optiques a permis le développement d’un large éventail de technologies correctrices. L’objectif est toujours le même : faire en sorte que les rayons lumineux se focalisent à nouveau sur la rétine, idéalement au niveau de la fovéa, et avec le moins d’aberrations possible. Selon le profil réfractif, l’âge, les attentes visuelles et l’état des structures oculaires, différentes stratégies peuvent être proposées, allant de la simple paire de lunettes à la chirurgie réfractive personnalisée.
Les lunettes restent la solution la plus répandue et la plus modulable : les verres sphériques corrigent la myopie et l’hypermétropie, les verres toriques corrigent l’astigmatisme, et les verres progressifs ou à double foyer compensent la presbytie. Les lentilles de contact offrent une correction plus proche de la cornée, ce qui peut améliorer la qualité de vision, notamment dans certains astigmatismes irréguliers ou après chirurgie. Des lentilles rigides perméables au gaz ou des lentilles sclérales sont parfois utilisées pour remodeler le front d’onde cornéen et réduire des aberrations complexes.
La chirurgie réfractive, principalement par laser (LASIK, PKR, SMILE), agit en remodelant la courbure de la cornée pour ajuster sa puissance dioptrique. Les plateformes de traitement modernes intègrent les mesures topographiques et aberrométriques pour proposer des ablations « personnalisées », visant non seulement à corriger la sphère et le cylindre, mais aussi à réduire certaines aberrations de haut degré. D’autres approches, comme les implants phakes (lenticules intraoculaires ajoutés sans enlever le cristallin) ou le remplacement du cristallin clair par un implant multifocal ou à profondeur de champ étendue (EDOF), permettent de corriger des myopies ou hypermétropies importantes, avec ou sans presbytie associée.
Dans tous les cas, ces technologies s’appuient sur les mêmes principes fondamentaux : la loi de Snell-Descartes, la notion de vergence, l’équilibre entre puissance cornéenne et longueur axiale, et la gestion des aberrations optiques. C’est en comprenant comment les rayons lumineux sont déviés et focalisés dans l’œil que l’on peut concevoir des solutions de plus en plus précises, capables d’optimiser non seulement l’acuité visuelle, mais aussi la qualité subjective de vision au quotidien — contraste, perception nocturne, confort visuel prolongé. En fin de compte, chaque correction, qu’elle soit optique ou chirurgicale, n’est rien d’autre qu’une façon de redessiner le chemin de la lumière jusqu’à votre rétine.