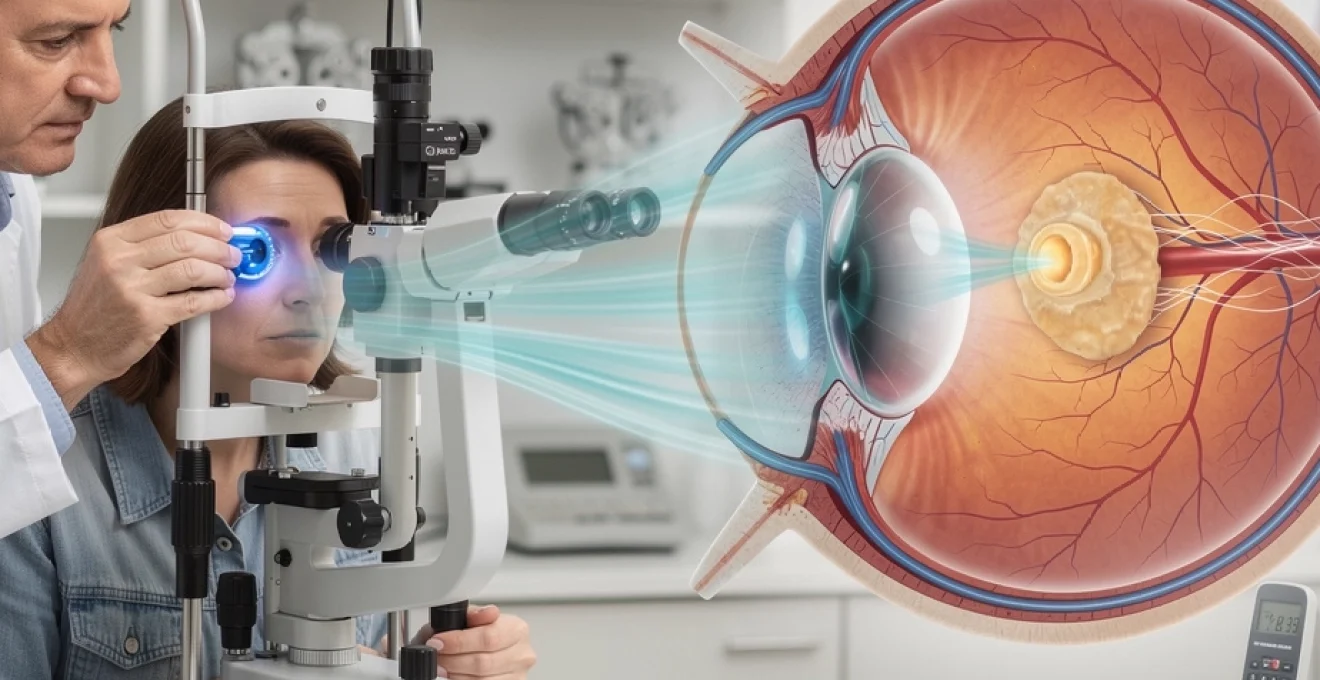
La pression intraoculaire élevée représente l’un des principaux facteurs de risque de perte visuelle irréversible dans le monde. Cette augmentation anormale de la pression exercée par l’humeur aqueuse à l’intérieur du globe oculaire peut entraîner des dommages progressifs et silencieux du nerf optique, conduisant potentiellement au glaucome, première cause de cécité irréversible en France. Comprendre les mécanismes complexes qui régissent cette pression et ses conséquences sur les structures oculaires devient essentiel pour tout professionnel de santé impliqué dans la préservation de la vision. L’hypertonie oculaire touche environ 3 à 4% de la population adulte de plus de 40 ans, mais seule une personne sur dix développera effectivement un glaucome. Cette disparité souligne l’importance d’une approche nuancée dans l’évaluation du risque individuel.
Mécanismes physiologiques de la pression intraoculaire et équilibre de l’humeur aqueuse
La pression intraoculaire normale, comprise entre 10 et 21 mmHg, résulte d’un équilibre délicat entre la production et l’évacuation de l’humeur aqueuse. Ce liquide transparent, produit en permanence, maintient non seulement la forme sphérique de l’œil mais assure également la nutrition des structures avasculaires comme la cornée et le cristallin. L’équilibre dynamique de ce système peut être comparé à un évier où l’eau arrive par le robinet tandis qu’elle s’évacue par la bonde : toute perturbation de ce système peut entraîner une accumulation excessive du liquide.
Production d’humeur aqueuse par les corps ciliaires et processus de sécrétion
Les corps ciliaires, situés derrière l’iris, constituent la principale source de production d’humeur aqueuse. Ces structures sécrètent environ 2 à 3 microlitres par minute grâce à trois mécanismes distincts : la sécrétion active, l’ultrafiltration et la diffusion passive. Le processus de sécrétion active, médié par l’enzyme anhydrase carbonique, représente près de 80% de la production totale d’humeur aqueuse. Cette production suit un rythme circadien marqué, avec une diminution nocturne d’environ 50% par rapport aux valeurs diurnes.
Voies d’évacuation conventionnelles : trabéculum et canal de schlemm
L’évacuation de l’humeur aqueuse s’effectue principalement par la voie trabéculaire conventionnelle, qui représente environ 75% du drainage total chez l’adulte jeune. Le trabéculum, structure filtrante située dans l’angle irido-cornéen, fonctionne comme un tamis dont les mailles se resserrent progressivement vers le canal de Schlemm. Ce système de drainage peut subir des modifications structurelles avec l’âge, entraînant une résistance accrue à l’écoulement de l’humeur aqueuse. La trabéculopathie représente le mécanisme physiopathologique principal du glaucome primitif à angle ouvert.
Drainage uvéoscléral et voies d’évacuation non conventionnelles
La voie uvéosclérale constitue une alternative importante au drainage trabéculaire, particulièrement chez le sujet jeune où elle peut représenter jusqu’à 50% de l’évacuation totale. Cette voie permet à l’humeur aqueuse de traverser les espaces intercellulaires du muscle ciliaire pour rejoindre l’espace sup
pace suprachoroïdien, puis de diffuser à travers la sclère vers la circulation veineuse épisclérale. Contrairement à la voie trabéculaire, ce drainage uvéoscléral est relativement indépendant de la pression intraoculaire, ce qui en fait une cible thérapeutique privilégiée. De nombreux collyres hypotonisants, notamment les analogues des prostaglandines, exercent leur effet en augmentant cette voie d’évacuation non conventionnelle. Avec l’avancée en âge et certaines pathologies, la perméabilité de ces tissus diminue, réduisant cette « soupape » naturelle et contribuant à l’élévation chronique de la pression intraoculaire.
Régulation circadienne de la PIO et variations nycthémérales
La pression intraoculaire (PIO) n’est pas un paramètre figé : elle fluctue au cours des 24 heures selon un rythme nycthéméral. Chez de nombreux patients, les valeurs les plus élevées sont observées tôt le matin ou pendant la nuit, parfois en dehors des horaires habituels de consultation. Ces variations sont liées à la sécrétion hormonale (cortisol, mélatonine), aux modifications de la posture, à la pression veineuse épisclérale et aux changements de la production d’humeur aqueuse. Ainsi, un patient peut présenter une PIO « normale » en consultation, alors que des pics tensionnels nocturnes suffisent à léser progressivement le nerf optique.
Cette dimension dynamique explique l’intérêt des courbes tensionnelles sur 24 heures ou des mesures répétées pour affiner l’évaluation du risque glaucomateux. Vous l’aurez compris : ce n’est pas seulement le « chiffre » de pression à un instant T qui compte, mais aussi l’amplitude des variations et la durée d’exposition à une pression intraoculaire élevée. Les personnes présentant de grandes fluctuations journalières de PIO, même dans la « norme », semblent plus à risque que celles dont la pression est modérément élevée mais stable.
Pathophysiologie du glaucome primitif à angle ouvert et altérations du nerf optique
Dans le glaucome primitif à angle ouvert, l’élévation de la pression intraoculaire agit comme un stress mécanique et métabolique chronique sur le nerf optique et les cellules ganglionnaires rétiniennes. L’angle irido-cornéen reste anatomiquement ouvert, mais le filtre trabéculaire est « encrassé », ce qui entraîne une hypertonie oculaire persistante. Pourtant, tous les patients avec pression intraoculaire élevée ne développent pas de glaucome, et certains glaucomes surviennent à pression dite « normale ». Comment expliquer ce paradoxe apparent ? Les modèles actuels combinent plusieurs hypothèses complémentaires : dommages mécaniques directs, ischémie microvasculaire et vulnérabilité intrinsèque des neurones rétiniens.
Excavation papillaire progressive et atteinte des fibres ganglionnaires
Le nerf optique quitte l’œil au niveau de la papille optique, zone où convergent les axones des cellules ganglionnaires rétiniennes. Sous l’effet d’une pression intraoculaire élevée prolongée, on observe une excavation papillaire progressive : la tête du nerf optique se creuse, comme un sol meuble soumis à une pression excessive. Ce phénomène traduit une perte irréversible de fibres nerveuses et une réorganisation de la tête du nerf optique. Au fond d’œil, l’ophtalmologiste évalue ce creusement par le rapport cup/disc (excavation/papille), paramètre central du diagnostic de glaucome.
Cliniquement, la destruction des cellules ganglionnaires se manifeste d’abord par des altérations subtiles du champ visuel périphérique, imperceptibles pour le patient. C’est un peu comme si l’on rognait progressivement les bords d’une photographie sans toucher au centre : tant que la vision centrale est préservée, la gêne fonctionnelle reste minime. Lorsque les lésions atteignent la zone maculaire, le handicap visuel devient majeur, mais la marge de manœuvre thérapeutique est alors très réduite. D’où l’importance de dépister les modifications structurelles papillaire et rétiniennes avant l’apparition de symptômes.
Théorie vasculaire : ischémie du nerf optique et perfusion oculaire
La théorie vasculaire postule que le glaucome primitif à angle ouvert résulte en partie d’une perfusion insuffisante du nerf optique. Le paramètre clé ici est la pression de perfusion oculaire, approximativement égale à la différence entre la pression artérielle moyenne et la pression intraoculaire. Si la pression artérielle est basse (par exemple chez un sujet hypotendu, ou en cas de chute nocturne excessive), une pression intraoculaire normale ou modérément augmentée peut suffire à réduire de façon critique l’apport sanguin au nerf optique. À l’inverse, une hypertension artérielle mal contrôlée peut altérer la microcirculation et accentuer la susceptibilité à l’ischémie.
Certains profils de patients illustrent particulièrement cette vulnérabilité vasculaire : migraines chroniques, syndrome de Raynaud, apnée du sommeil, hypotension nocturne marquée ou dysautonomie. Dans ces contextes, la pression intraoculaire élevée n’est pas le seul « coupable », mais elle contribue à franchir un seuil au-delà duquel la perfusion devient insuffisante. On comprend ainsi pourquoi, à pression intraoculaire équivalente, deux individus n’auront pas le même risque de glaucome : tout dépend de la réserve vasculaire de leur nerf optique.
Théorie mécanique : compression axonale et dysfonction mitochondriale
La théorie mécanique met l’accent sur la déformation de la lame criblée, structure perforée à travers laquelle passent les axones du nerf optique. Une pression intraoculaire élevée chronique induit une déformation postérieure de cette lame, entraînant un « coude » et une compression des fibres axonales. Ce phénomène est comparable à un câble électrique qui serait plié et écrasé au même endroit jour après jour : la conduction est d’abord ralentie, puis les fils internes finissent par rompre. Cette compression perturbe le transport axonal des nutriments et des facteurs trophiques essentiels à la survie des cellules ganglionnaires.
Sur le plan cellulaire, cette agression mécanique s’accompagne d’une dysfonction mitochondriale, avec production accrue de radicaux libres et baisse de la capacité de production énergétique. Les cellules ganglionnaires, hautement dépendantes d’un métabolisme oxydatif efficace, entrent alors dans une phase de stress chronique qui les rend plus sensibles à la moindre variation de pression intraoculaire ou de perfusion. La combinaison des facteurs mécaniques et vasculaires crée un cercle vicieux de plus en plus difficile à enrayer sans réduction significative de la PIO.
Neuroprotection et cascade apoptotique des cellules ganglionnaires rétiniennes
Quelle que soit la porte d’entrée (mécanique ou vasculaire), le point final commun du glaucome est la mort programmée (apoptose) des cellules ganglionnaires rétiniennes. Sous l’effet du stress oxydatif, de la privation trophique et des perturbations ioniques, ces neurones activent des voies de signalisation pro-apoptotiques qui aboutissent à une fragmentation de l’ADN et à la disparition progressive des corps cellulaires. Contrairement à la nécrose, cette apoptose est silencieuse : pas d’inflammation majeure, pas de douleur, ce qui explique le caractère trompeusement asymptomatique du glaucome chronique.
Face à cette cascade apoptotique, le concept de neuroprotection s’est imposé comme un axe de recherche majeur. Au-delà de la simple réduction de la pression intraoculaire, l’objectif est de préserver la viabilité des cellules ganglionnaires en modulant le stress oxydatif, l’excitotoxicité glutamatergique ou les voies inflammatoires. Certaines molécules (brimonidine, antagonistes du NMDA, facteurs de croissance) ont montré des effets neuroprotecteurs expérimentaux, mais leur traduction clinique reste limitée. Dans la pratique actuelle, la meilleure neuroprotection reste un contrôle tensionnel strict, associé à la prise en charge des facteurs vasculaires et systémiques.
Valeurs seuils de pression intraoculaire et facteurs de risque associés
On considère classiquement qu’une pression intraoculaire « normale » se situe entre 10 et 21 mmHg. Pourtant, des études de cohorte ont montré que certains patients développent un glaucome avec des pressions inférieures à 21 mmHg (glaucome à pression normale), tandis que d’autres ne présentent aucun dommage malgré des valeurs chroniquement supérieures à ce seuil. Comment interpréter alors une pression à 22, 24 ou 26 mmHg chez un patient donné ? La réponse repose sur l’analyse globale du profil de risque plutôt que sur un chiffre isolé.
Chez un adulte sans autre facteur de risque, une PIO légèrement élevée pourra parfois justifier une simple surveillance rapprochée. À l’inverse, chez un patient myope fort, d’origine africaine, avec des antécédents familiaux de glaucome et une cornée fine, une pression intraoculaire à 20 mmHg peut déjà être préoccupante. On parle alors de « pression cible » individualisée : la valeur de PIO à atteindre par le traitement pour limiter au maximum le risque de progression des lésions. Cette pression cible est d’autant plus basse que le glaucome est avancé ou que les facteurs de risque associés sont nombreux.
| Situation clinique | PIO mesurée | Interprétation probable |
|---|---|---|
| Adulte < 40 ans, sans facteur de risque | 22 mmHg | Hypertonie oculaire modérée, surveillance ou traitement selon contexte |
| Glaucome avéré, atteinte avancée du champ visuel | 18 mmHg | Pression encore trop élevée, abaissement supplémentaire nécessaire |
| Glaucome à pression normale suspecté | 15 mmHg | Pression « normale » mais inadéquate pour ce nerf optique fragile |
Les principaux facteurs de risque associés à une pression intraoculaire élevée et à la survenue de glaucome incluent l’âge (> 40–45 ans), les antécédents familiaux de glaucome, l’origine ethnique (sujets à peau noire ou d’origine antillaise), la myopie forte, la cornée fine, le diabète, l’hypertension artérielle et la prise prolongée de corticoïdes. En pratique, plus ces facteurs sont nombreux, plus l’« innocuité » d’une pression intraoculaire limite devient discutable. C’est précisément pour cela que vous ne trouverez pas de seuil universel applicable à tous, mais une approche graduée et personnalisée du risque.
Techniques de mesure tonométrique : goldman, pascal et tonomètres de rebond
La mesure précise de la pression intraoculaire est une étape clé de l’évaluation du risque glaucomateux. Plusieurs techniques coexistent, chacune avec ses avantages et ses limites. Le tonomètre de Goldmann, basé sur le principe d’aplanation de la cornée, reste la référence (« gold standard ») en pratique clinique. Il nécessite une anesthésie locale et l’utilisation d’un colorant (fluorescéine) pour visualiser l’anneau d’aplanation. Bien utilisé, il offre une bonne reproductibilité, mais sa précision est influencée par l’épaisseur et la rigidité cornéennes.
Les tonomètres à air (ou tonométrie non contact), très répandus en dépistage, projettent un jet d’air sur la cornée et mesurent la force nécessaire pour l’aplanir. Ils sont rapides, indolores et ne nécessitent pas de contact direct, ce qui en fait un outil pratique pour les examens de masse. Cependant, leur précision est un peu moindre, surtout pour les pressions très élevées ou très basses, et ils restent sensibles aux propriétés biomécaniques de la cornée. C’est pourquoi un résultat anormal en tonométrie à air doit idéalement être confirmé par une mesure de Goldmann.
La tonométrie dynamique de contour (tonomètre de Pascal) a été développée pour réduire l’influence de l’épaisseur cornéenne en épousant la courbure de la cornée plutôt qu’en l’aplatissant. Cette technique fournit une estimation plus proche de la « vraie » pression intraoculaire et permet une mesure pulsatile continue, donnant des informations complémentaires sur la dynamique vasculaire oculaire. Les tonomètres de rebond, quant à eux, utilisent une petite sonde qui vient effleurer plusieurs fois la cornée ; très portables et ne nécessitant pas de collyre anesthésique, ils s’avèrent utiles pour le suivi à domicile ou chez l’enfant.
Pour interpréter correctement une pression intraoculaire, il est indispensable de tenir compte de l’épaisseur cornéenne centrale, mesurée par pachymétrie. Une cornée très épaisse tend à surestimer la PIO réelle, tandis qu’une cornée fine la sous-estime. Sans cette information, on risque de classer à tort certains patients en hypertonie oculaire ou, au contraire, de méconnaître une pression pathologiquement élevée. En pratique, votre ophtalmologiste croise toujours la mesure tonométrique avec les données de pachymétrie, de fond d’œil et de champ visuel pour poser un diagnostic fiable.
Conséquences cliniques de l’hypertonie oculaire sur les structures intraoculaires
L’hypertonie oculaire prolongée n’affecte pas uniquement le nerf optique : l’ensemble des structures intraoculaires subit les effets d’une pression anormalement élevée. Au niveau de la cornée, une pression très importante et aiguë peut entraîner un œdème cornéen, responsable d’une vision floue et de halos colorés autour des sources lumineuses, typiques des crises aiguës par fermeture de l’angle. À l’inverse, dans les hypertonies chroniques modérées, la cornée peut rester claire et asymptomatique, renforçant l’illusion d’un œil « en bonne santé ».
La rétine et la choroïde subissent également les répercussions d’une pression intraoculaire élevée, via une altération de la perfusion et une compression des capillaires. Dans certaines situations extrêmes, une hypertonie majeure peut conduire à un véritable collapse de la circulation rétinienne. Plus subtilement, des hypertonies modérées mais persistantes favorisent une neuropathie optique glaucomateuse lente, dont la signature la plus caractéristique reste la réduction concentrique du champ visuel. Là encore, le patient ne perçoit souvent rien tant que la vision centrale et la lecture restent intactes.
Paradoxalement, une baisse excessive et non contrôlée de la pression intraoculaire (hypotonie) peut également être délétère, surtout après chirurgie filtrante trop efficace. Une PIO trop basse peut provoquer des plis de la choroïde, un œdème maculaire ou une baisse durable d’acuité visuelle. On voit bien ici que l’objectif n’est pas d’obtenir la pression la plus basse possible à tout prix, mais d’atteindre une zone de sécurité adaptée à chaque œil. Cette recherche d’équilibre est au cœur de la stratégie thérapeutique.
Stratégies thérapeutiques de contrôle pressionnelle : collyres hypotonisants et chirurgie filtrante
Réduire la pression intraoculaire est aujourd’hui le seul levier thérapeutique démontré pour ralentir l’évolution du glaucome et prévenir la perte visuelle. Les stratégies disponibles se répartissent en trois grandes catégories : traitements médicamenteux (principalement par collyres), traitements par laser et interventions chirurgicales filtrantes ou de drainage. Le choix entre ces options dépend du niveau de pression à atteindre, de la sévérité du glaucome, de l’âge du patient, mais aussi de sa capacité à suivre un traitement au long cours.
Les collyres hypotonisants constituent le traitement de première ligne dans la majorité des cas. Les analogues des prostaglandines (latanoprost, bimatoprost, travoprost…) augmentent principalement le drainage uvéoscléral et permettent une baisse de la PIO souvent supérieure à 25–30 %. Les bêtabloquants (timolol, cartéolol) réduisent la production d’humeur aqueuse par les corps ciliaires. Les inhibiteurs de l’anhydrase carbonique (dorzolamide, brinzolamide) et les agonistes alpha-2 (brimonidine) agissent aussi en diminuant la sécrétion d’humeur aqueuse, parfois avec un léger effet sur l’élimination. Enfin, la pilocarpine, moins utilisée aujourd’hui, augmente l’écoulement trabéculaire en contractant le muscle ciliaire.
Lorsque les collyres ne suffisent pas à atteindre la pression cible, ou en cas d’intolérance, les techniques au laser offrent une alternative intéressante. La trabéculoplastie sélective (SLT) cible spécifiquement le trabéculum pour en améliorer la perméabilité, un peu comme si l’on « détartrait » un filtre encrassé. Elle peut être proposée d’emblée chez certains patients en alternative aux gouttes, ou en complément quand la pression reste insuffisamment contrôlée. Les iridotomies périphériques au laser, quant à elles, sont réservées aux glaucomes par fermeture de l’angle ou aux angles étroits à risque.
En dernier recours, ou lorsque la maladie progresse malgré un traitement médical et laser optimal, la chirurgie filtrante entre en jeu. La trabéculectomie et les sclérectomies profondes non perforantes créent une voie d’évacuation supplémentaire sous la conjonctive, formant une « bulle de filtration » qui joue le rôle de soupape permanente. Des dispositifs mini-invasifs (MIGS, pour Micro-Invasive Glaucoma Surgery) et des implants de drainage complètent désormais l’arsenal, offrant des options plus ciblées et parfois plus sûres. Chaque technique comporte des risques (hypotonie, infection, cicatrisation excessive), ce qui justifie une évaluation soigneuse du rapport bénéfice/risque pour chaque patient.
Au-delà de la technique choisie, la réussite à long terme repose sur deux piliers : un suivi régulier (fond d’œil, champ visuel, OCT, tonométrie) et une bonne observance thérapeutique. Vous pouvez disposer du meilleur collyre du monde, il restera inefficace s’il n’est pas instillé régulièrement. À l’inverse, un patient bien informé, impliqué dans sa prise en charge et suivi de manière structurée a de grandes chances de conserver une vision satisfaisante tout au long de sa vie, même en présence d’une pression intraoculaire élevée initialement.