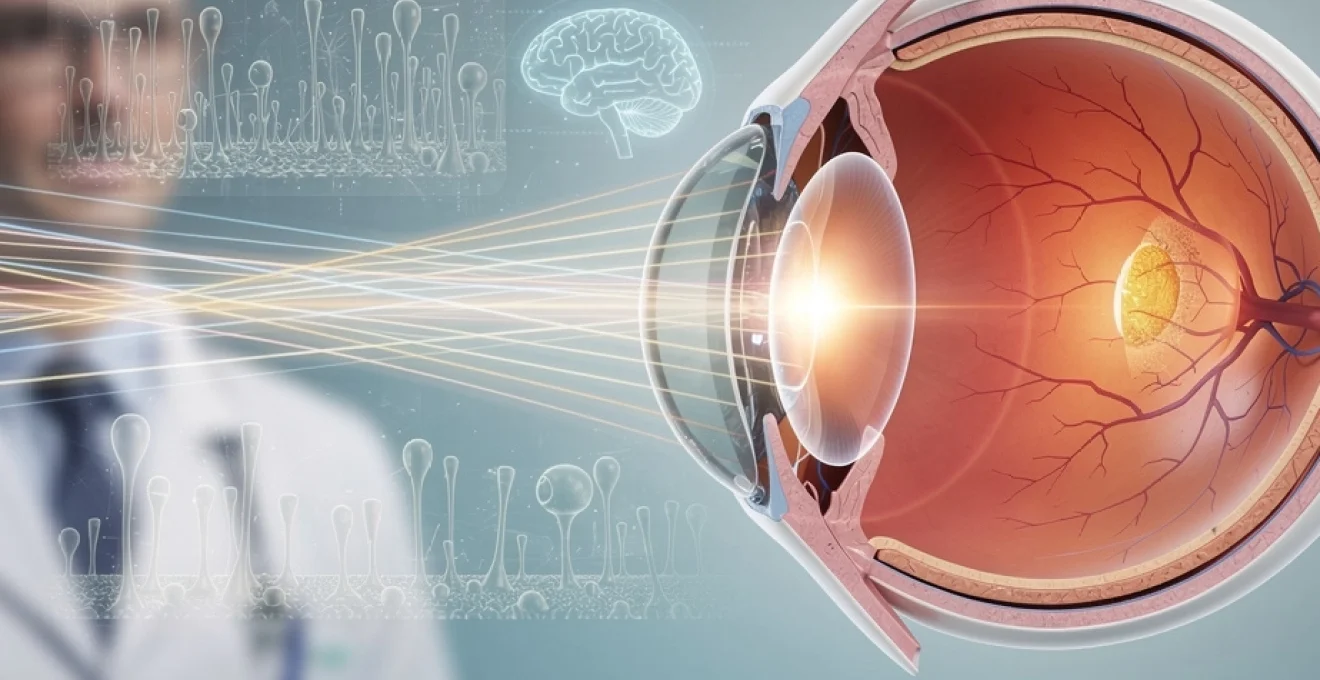
L’œil humain représente l’un des systèmes optiques les plus sophistiqués de la nature, capable de traiter instantanément des millions d’informations lumineuses pour créer la perception visuelle. Ce globe oculaire de 2,4 centimètres de diamètre et pesant seulement 7 grammes constitue un véritable concentré de technologie biologique. Sa capacité à s’adapter automatiquement aux variations de luminosité, à effectuer une mise au point précise sur des objets situés à différentes distances et à discriminer plus de 10 millions de nuances colorées dépasse largement les performances des caméras les plus avancées. La compréhension de ce mécanisme complexe nécessite d’explorer l’architecture anatomique remarquable de l’appareil visuel, les phénomènes physiques de réfraction qui gouvernent la formation des images, ainsi que les processus biochimiques sophistiqués de conversion photochimique qui transforment la lumière en influx nerveux.
Architecture anatomique de l’appareil visuel humain
L’appareil visuel humain s’organise selon une structure concentrique complexe, où chaque composant joue un rôle spécifique dans le processus de vision. Cette organisation stratifiée permet une optimisation remarquable de la transmission lumineuse et de la formation d’images nettes sur la rétine. L’ensemble fonctionne comme un système optique intégré, où la moindre modification d’un élément peut affecter significativement la qualité de la vision.
Structure stratifiée de la cornée et coefficient de réfraction
La cornée constitue la première interface optique du système visuel, avec ses cinq couches distinctes qui assurent à la fois la protection et la réfraction primaire de la lumière. L’épithélium antérieur, d’une épaisseur de 50 micromètres, se régénère continuellement tous les 7 à 10 jours grâce aux cellules souches du limbe scléro-cornéen. Cette capacité de régénération exceptionnelle maintient la transparence cornéenne essentielle à une vision claire.
Le stroma cornéen, représentant 90% de l’épaisseur totale, présente une organisation lamellaire unique avec ses 200 à 300 couches de fibres de collagène disposées selon des orientations précises. Cette architecture confère à la cornée un indice de réfraction de 1,376, générant une puissance dioptrique d’environ 43 dioptries, soit les deux tiers du pouvoir réfractif total de l’œil. La membrane de Descemet et l’endothélium postérieur régulent quant à eux l’hydratation cornéenne par un mécanisme de pompage actif, maintenant la teneur en eau à 78% pour préserver la transparence optimale.
Géométrie cristallinienne et mécanisme d’accommodation
Le cristallin présente une structure lenticulaire biconvexe d’une complexité remarquable, composé de plus de 2000 fibres cristalliniennes disposées en couches concentriques. Cette lentille biologique de 4 millimètres d’épaisseur possède un indice de réfraction variable, allant de 1,386 en périphérie à 1,406 au centre, créant naturellement un gradient optique qui minimise les aberrations sphériques.
Le processus d’accommodation repose sur la contraction coordonnée des muscles ciliaires qui modifient la tension exercée sur les fibres zonulaires. Lorsque ces muscles se contractent pour la vision de près, ils relâchent la tension zonulaire, permettant au cristallin de se bomber sous l’effet de son élasticité naturelle. Cette déformation augmente sa puissance réfractive de
plusieurs dioptries, jusqu’à environ 14 à 16 dioptries chez l’adulte jeune. À l’inverse, pour la vision de loin, les muscles ciliaires se relâchent, la tension zonulaire augmente et le cristallin s’aplatit, réduisant sa puissance optique. Ce mécanisme d’accommodation, comparable à l’autofocus d’un objectif d’appareil photo, permet de maintenir l’image nette sur la rétine malgré les variations de distance des objets observés. Avec l’âge, l’élasticité du cristallin diminue progressivement, entraînant une réduction de l’amplitude accommodative qui se manifeste cliniquement par la presbytie.
Composition vitréenne et transmission lumineuse
Le corps vitré occupe environ deux tiers du volume du globe oculaire et se présente sous la forme d’un gel transparent, composé à plus de 98% d’eau. Cette matrice aqueuse est structurée par un réseau de fibres de collagène de type II et d’acide hyaluronique, conférant au vitré sa consistance viscoélastique. Sa transparence est essentielle pour la bonne transmission de la lumière vers la rétine et dépend d’un agencement homogène des fibrilles et d’une faible concentration en protéines.
Sur le plan optique, l’indice de réfraction du corps vitré est d’environ 1,336, très proche de celui de l’humeur aqueuse, ce qui limite les phénomènes de réflexion interne et de diffusion de la lumière. Le vitré joue également un rôle mécanique en maintenant la rétine appliquée contre l’épithélium pigmentaire et la choroïde, ce qui garantit une bonne qualité d’image rétinienne. Avec le vieillissement, le processus de synérèse vitréenne conduit à une liquéfaction partielle du gel et à l’apparition de condensations fibrillaires, perçues comme des « mouches volantes » ou myodésopsies par le patient.
Le corps vitré participe enfin à l’amortissement des chocs et des micro-mouvements oculaires, stabilisant ainsi la projection de l’image sur la rétine. Cette stabilité est indispensable pour une vision fine, notamment au niveau de la fovéa centralis où la densité de photorécepteurs est maximale. Toute opacification vitréenne significative, telle qu’un hémorragie ou une inflammation, peut altérer la transmission lumineuse et dégrader fortement l’acuité visuelle.
Organisation rétinienne en couches cellulaires spécialisées
La rétine constitue la couche nerveuse la plus interne de l’œil et se compose de dix couches histologiques superposées, depuis l’épithélium pigmentaire rétinien jusqu’à la couche des fibres nerveuses. Cette organisation stratifiée permet un traitement précoce et sophistiqué de l’information visuelle avant même son relais vers le cerveau. On distingue notamment la couche des photorécepteurs (cônes et bâtonnets), la couche nucléaire externe, la couche plexiforme externe, la couche nucléaire interne et la couche plexiforme interne.
Les cônes, concentrés dans la région maculaire et particulièrement dans la fovéa, assurent la vision photopique (de jour), la perception des couleurs et la haute acuité visuelle. Les bâtonnets, majoritaires en périphérie rétinienne, sont spécialisés dans la vision scotopique (en faible luminosité) et la détection des mouvements. Les signaux issus de ces photorécepteurs sont relayés par les cellules bipolaires, horizontales et amacrines qui assurent un premier niveau d’intégration et de modulation de l’information lumineuse.
Les cellules ganglionnaires, dont les axones forment le nerf optique, représentent le dernier maillon rétinien avant l’envoi des signaux au cerveau. Leur organisation en champs récepteurs de type centre-périphérie permet une analyse fine des contrastes et des contours. Ainsi, loin d’être un simple « écran de projection », la rétine se comporte comme un véritable processeur d’images, réalisant une compression et un filtrage avancés de l’information avant sa transmission le long des voies optiques.
Phénomènes de réfraction et formation de l’image rétinienne
Pour comprendre le fonctionnement optique de l’œil humain, il est indispensable d’analyser comment les rayons lumineux sont déviés à travers les différents milieux transparents. La cornée, l’humeur aqueuse, le cristallin et le corps vitré possèdent chacun un indice de réfraction spécifique qui conditionne la trajectoire des rayons. L’œil emmétrope est ainsi conçu pour focaliser, au repos accommodatif, les rayons parallèles provenant de l’infini directement sur la rétine, et plus précisément au niveau de la fovéa, afin de produire une image nette et inversée.
Lois de Snell-Descartes appliquées au système oculaire
Les lois de Snell-Descartes décrivent la relation entre les angles d’incidence et de réfraction lorsqu’un rayon lumineux traverse deux milieux d’indices différents. Dans l’œil, ces lois s’appliquent principalement aux interfaces air-cornée, cornée-humeur aqueuse et humeur aqueuse-cristallin. À chaque interface, la direction du rayon est modifiée en fonction du rapport des indices de réfraction et de l’angle d’incidence, ce qui concourt à la focalisation finale sur la rétine.
La cornée, avec son indice de 1,376, est la surface la plus réfringente car le contraste avec l’air (indice ≈ 1,0) est maximal. C’est pourquoi elle apporte la plus grande part de la puissance dioptrique de l’œil, bien avant le cristallin. En revanche, les interfaces internes (humeur aqueuse-cristallin, cristallin-vitré) présentent des différences d’indices plus modestes, induisant des changements de direction plus subtils mais essentiels pour le réglage fin de la mise au point.
On peut assimiler le système optique oculaire à une lentille épaisse composée de plusieurs dioptres successifs. Lorsque vous fixez un objet, les rayons issus de chaque point de cet objet sont réfractés de manière à converger vers un point précis de la rétine. Si la convergence se fait en avant ou en arrière de celle-ci, un flou apparaît, illustrant des défauts de réfraction tels que la myopie ou l’hypermétropie.
Calcul dioptrique et distance focale du système optique
La puissance optique d’un système se mesure en dioptries (D), unité définie comme l’inverse de la distance focale exprimée en mètres. Chez l’œil humain emmétrope, la puissance totale au repos accommodatif se situe autour de 60 dioptries. La cornée contribue en moyenne à 43 D, tandis que le cristallin ajoute environ 17 D, modulables en fonction de l’accommodation. Ainsi, la distance focale globale de l’œil est d’environ 16,7 mm, correspondant à la distance entre le centre optique effectif et la rétine.
En pratique, le calcul dioptrique du système oculaire tient compte de la position des plans principaux et de l’épaisseur des différents milieux. Les opticiens et ophtalmologistes utilisent ces paramètres pour déterminer la correction nécessaire lorsque la puissance de l’œil ne permet pas de focaliser correctement l’image sur la rétine. Une erreur réfractive de seulement 1 dioptrie suffit, par exemple, à réduire nettement la netteté des objets éloignés.
Vous vous demandez peut-être comment ces valeurs se traduisent au quotidien ? Lorsque l’on prescrit des lunettes de -2,00 D à un patient myope, on compense une puissance excessive du système oculaire en interposant une lentille divergente. Inversement, une correction de +3,00 D pour un hypermétrope renforce la convergence des rayons afin de ramener le foyer sur le plan rétinien. Tout l’enjeu est de reconstituer un système optique équivalent à l’œil emmétrope idéal.
Aberrations chromatiques et sphériques de l’œil emmétrope
Comme tout système optique réel, l’œil humain n’est pas exempt d’aberrations. Les aberrations sphériques surviennent parce que les rayons passant par la périphérie de la cornée ou du cristallin ne convergent pas exactement au même point que ceux proches de l’axe optique. Théoriquement, cela devrait dégrader la netteté de l’image, en particulier pour les grandes pupilles. Cependant, la présence d’un gradient d’indice dans le cristallin et la diminution automatique du diamètre pupillaire en forte luminosité réduisent significativement cette aberration.
Les aberrations chromatiques, quant à elles, résultent du fait que l’indice de réfraction des milieux oculaires varie légèrement selon la longueur d’onde de la lumière. Les rayons bleus (courte longueur d’onde) sont davantage déviés que les rayons rouges (longue longueur d’onde), ce qui produit une focalisation à des plans légèrement différents. L’œil présente ainsi une aberration chromatique longitudinale de l’ordre de 1 dioptrie entre le bleu et le rouge.
Heureusement, le système visuel compense en grande partie ces imperfections grâce à des mécanismes neuronaux sophistiqués qui optimisent la perception des contrastes et des contours. On peut comparer cette situation à un appareil photo numérique dont le capteur et le logiciel de traitement corrigent les limites optiques de l’objectif. Les chercheurs en optique adaptative utilisent aujourd’hui des techniques de mesure des aberrations de haut degré pour concevoir des lentilles et des implants intraoculaires de plus en plus performants, rapprochant la vision clinique de l’œil de la performance théorique maximale.
Processus d’inversion et projection sur la fovéa centralis
Lorsqu’un objet est observé, chaque point émet (ou réfléchit) des rayons lumineux qui, après réfraction, se croisent au niveau du plan focal oculaire. Ce croisement entraîne une inversion de l’image : le haut de la scène se retrouve projeté vers le bas de la rétine et la droite vers la gauche. Ainsi, l’image rétinienne est systématiquement inversée et légèrement réduite par rapport à la scène réelle. C’est le cerveau, via le cortex visuel, qui réinterprète et « redresse » cette information pour nous donner une perception cohérente du monde.
La fovéa centralis, située au centre de la macula lutea, représente la zone de plus haute résolution visuelle. D’un diamètre d’environ 1,5 mm, elle contient une densité maximale de cônes (jusqu’à 200 000 par mm²) et est dépourvue de bâtonnets. La structure fovéale, avec un amincissement des couches internes de la rétine, minimise la dispersion de la lumière et permet une projection quasi directe des rayons sur les photorécepteurs.
Lorsque vous fixez un détail précis, comme une lettre sur un écran ou le visage d’une personne, l’ensemble du système oculomoteur oriente le globe de sorte que l’image de ce point d’intérêt se forme sur la fovéa. C’est ce que l’on appelle la fixation fovéale. En périphérie, la résolution diminue mais la sensibilité au mouvement augmente, ce qui illustre un compromis évolutif optimal entre acuité et vigilance. Sans cette organisation centrée autour de la fovéa centralis, la lecture fine ou la reconnaissance faciale telle que nous la connaissons serait impossible.
Phototransduction rétinienne et cascade enzymatique
Au-delà des phénomènes purement optiques, le fonctionnement de l’œil humain repose sur une étape clé : la conversion de l’énergie lumineuse en signal électrique. Ce processus, appelé phototransduction, se déroule au niveau des segments externes des photorécepteurs et implique une cascade enzymatique d’une grande précision. En quelques millisecondes, un photon absorbé par un pigment visuel déclenche une suite de réactions biochimiques qui aboutissent à une modification du potentiel de membrane de la cellule.
Activation de la rhodopsine par photoisomérisation
La rhodopsine, pigment visuel des bâtonnets, est composée d’une opsine (protéine transmembranaire) et d’un chromophore, le 11-cis-rétinal, dérivé de la vitamine A. Lorsqu’un photon frappe le segment externe d’un bâtonnet, il est absorbé par la rhodopsine, provoquant une photoisomérisation du 11-cis-rétinal en all-trans-rétinal. Ce changement de conformation, bien que minime à l’échelle moléculaire, suffit à transformer la rhodopsine en une forme activée appelée métarhodopsine II.
La métarhodopsine II agit comme un véritable interrupteur biologique en activant une protéine G spécifique, la transducine. Fait remarquable, un seul photon peut activer plusieurs centaines de molécules de transducine, illustrant le caractère amplificateur de la cascade de phototransduction. C’est cette amplification qui explique la sensibilité extrême des bâtonnets, capables de répondre à des niveaux de lumière extrêmement faibles, proches de la limite physique de détection.
On peut comparer ce mécanisme à un détecteur d’alarme ultra-sensible : un infime signal d’entrée (un photon unique) déclenche une réaction en chaîne qui se propage et se renforce à chaque étape. Sans cette amplification, la vision nocturne serait largement insuffisante pour nous permettre de nous orienter dans des conditions de faible luminosité.
Voie des photorécepteurs cônes et vision photopique
Les cônes, responsables de la vision photopique et de la perception des couleurs, possèdent des pigments visuels appelés opsines côniques. On distingue trois types principaux de cônes chez l’humain trichromate : les cônes L (sensibles aux grandes longueurs d’onde, rouge), les cônes M (moyennes longueurs d’onde, vert) et les cônes S (courtes longueurs d’onde, bleu). Chaque type de cône exprime une opsine différente, ajustée pour absorber préférentiellement une bande spécifique du spectre lumineux.
La cascade de phototransduction dans les cônes est globalement similaire à celle des bâtonnets, impliquant une photoisomérisation du 11-cis-rétinal et l’activation d’une transducine cônique. Toutefois, les cinétiques de réponse sont plus rapides et la sensibilité individuelle des cônes est moindre, ce qui permet une adaptation optimale à des conditions de forte luminosité. C’est grâce à cette organisation que nous pouvons distinguer des détails fins et différencier plus de 10 millions de nuances colorées en plein jour.
Lorsque vous observez un paysage coloré, chaque point de la scène stimule différemment les cônes L, M et S. Le cerveau compare ensuite ces signaux relatifs pour reconstituer la teinte, la saturation et la luminosité perçues. Ce codage trichromatique, mis en évidence dès le XIXᵉ siècle par Young et Helmholtz, constitue l’un des fondements de la colorimétrie moderne, utilisée aujourd’hui dans la conception des écrans et des systèmes d’éclairage LED.
Mécanisme de transduction des bâtonnets en vision scotopique
En conditions de faible luminosité, ce sont les bâtonnets qui prennent le relais et assurent la vision scotopique. Ils sont environ 120 millions dans chaque œil et leur densité augmente vers la périphérie rétinienne, expliquant pourquoi nous percevons parfois mieux un objet très sombre en le regardant légèrement de côté. Leur organisation en réseaux convergents vers les cellules bipolaires et ganglionnaires amplifie encore la sensibilité, au prix d’une diminution de la résolution spatiale.
Au repos, dans l’obscurité, la membrane du segment externe des bâtonnets est relativement dépolarisée (environ -40 mV) en raison de l’ouverture de canaux cationiques contrôlés par le GMPc (guanosine monophosphate cyclique). L’entrée continue de Na⁺ et de Ca²⁺, appelée « courant sombre », maintient la cellule dans un état de libération tonique de glutamate au niveau de la synapse avec les cellules bipolaires. Lorsqu’un photon est absorbé et que la cascade de phototransduction est activée, ce courant sombre est interrompu, conduisant à une hyperpolarisation de la cellule.
Sur le plan fonctionnel, cela signifie que, contrairement à de nombreux neurones, les photorécepteurs répondent à la lumière par une diminution de leur activité de sécrétion de neurotransmetteur. Ce renversement de logique peut sembler contre-intuitif, mais il permet une plus grande finesse de modulation dans la transmission du signal, notamment lorsque l’intensité lumineuse varie sur une large plage, allant de la nuit étoilée au plein soleil.
Cascade de la phosphodiestérase et hyperpolarisation cellulaire
La transducine activée par la métarhodopsine II stimule à son tour une enzyme clé : la phosphodiestérase spécifique du GMPc (PDE6). Cette enzyme hydrolyse rapidement le GMPc en GMP, provoquant une chute brutale de la concentration de GMPc dans le segment externe du photorécepteur. Or, les canaux cationiques dépendants du GMPc nécessitent la liaison de cette molécule pour rester ouverts.
La diminution du GMPc entraîne donc la fermeture progressive de ces canaux, ce qui réduit l’entrée de Na⁺ et de Ca²⁺ et provoque une hyperpolarisation de la membrane, pouvant atteindre -65 à -70 mV. Cette hyperpolarisation se propage jusqu’au segment interne et à la terminaison synaptique du photorécepteur, où elle modifie la libération de glutamate. Ainsi, l’activation d’une seule molécule de rhodopsine peut aboutir à la fermeture de plusieurs centaines de canaux, illustrant une nouvelle fois l’effet multiplicateur de la cascade enzymatique.
On peut comparer cette séquence à un système de dominos : la chute d’une première pièce (l’absorption d’un photon) déclenche la chute de nombreuses autres (activation de la transducine, de la PDE, fermeture des canaux, hyperpolarisation). L’efficacité et la rapidité de cette cascade sont telles que la réponse électrique peut être enregistrée en moins de 50 millisecondes après l’absorption du photon, ce qui contribue à la réactivité globale de notre système visuel.
Régénération du 11-cis-rétinal par l’épithélium pigmentaire
Après activation, le chromophore all-trans-rétinal doit être recyclé pour permettre une nouvelle capture de photons. Ce cycle visuel implique une série de réactions enzymatiques qui se déroulent entre les segments externes des photorécepteurs et l’épithélium pigmentaire rétinien (EPR). L’all-trans-rétinal est d’abord réduit en all-trans-rétinol, puis transporté vers l’EPR où il est estérifié et réisomérisé en 11-cis-rétinol, avant d’être reconverti en 11-cis-rétinal.
Le 11-cis-rétinal ainsi régénéré est ensuite renvoyé vers les photorécepteurs pour se recombiner avec l’opsine et reformer une nouvelle molécule de rhodopsine ou d’opsine cônique fonctionnelle. Ce cycle est énergétiquement coûteux et dépend de l’apport en vitamine A (rétinol) via la circulation sanguine choroïdienne. Un déficit prolongé en vitamine A peut donc entraîner des troubles de la vision nocturne (héméralopie), illustrant l’importance de la nutrition dans le maintien du fonctionnement optique de l’œil humain.
L’épithélium pigmentaire joue également un rôle crucial dans la phagocytose quotidienne des disques membranaires usés des segments externes et dans l’absorption de la lumière diffusée, limitant ainsi les réflexions internes parasites. Sans cet entretien permanent et cette régénération des pigments visuels, la sensibilité rétinienne déclinerait rapidement, compromettant la qualité de la vision tant diurne que nocturne.
Traitement neuronal de l’information visuelle
Une fois convertie en signal électrique au niveau des photorécepteurs, l’information lumineuse subit un traitement neuronal sophistiqué à plusieurs niveaux du système visuel. Dès la rétine, les cellules horizontales, bipolaires et amacrines réorganisent le flux d’informations en créant des circuits d’inhibition latérale et de convergence. Ce traitement précoce met en évidence les contrastes de luminance, les contours et certains mouvements, préparant ainsi des signaux déjà fortement structurés pour leur transmission vers le cerveau.
Les axones des cellules ganglionnaires forment le nerf optique, qui quitte le globe oculaire au niveau de la papille. Les deux nerfs optiques se rejoignent ensuite au chiasma optique, où les fibres issues de la moitié nasale de chaque rétine croisent la ligne médiane. Cette organisation permet de regrouper au niveau de chaque hémisphère cérébral les informations provenant du champ visuel controlatéral. Les fibres poursuivent leur trajet sous forme de tractus optiques jusqu’au corps genouillé latéral (CGL) du thalamus.
Au sein du CGL, véritable relais et centre de tri, les signaux sont distribués en couches distinctes, séparant notamment les voies parvocellulaire (détails fins et couleurs) et magnocellulaire (mouvements et contrastes de luminance). Les neurones du CGL projettent ensuite vers le cortex visuel primaire (V1) via les radiations optiques. Dans V1, les informations sont organisées en cartes topographiques précises, appelées cartes rétinotopiques, où chaque point du cortex correspond à une région spécifique de la rétine.
Le traitement ne s’arrête pas là : à partir de V1, l’information est redistribuée vers des aires visuelles secondaires et associatives le long de deux grandes voies fonctionnelles. La voie dorsale, ou « voie du où », projetant vers les lobes pariétaux, analyse la localisation spatiale, le mouvement et la coordination visuo-motrice. La voie ventrale, ou « voie du quoi », dirigée vers les lobes temporaux, se spécialise dans la reconnaissance des formes, des objets et des visages. C’est la coopération de ces multiples niveaux de traitement neuronal qui transforme l’image rétinienne brute en une perception consciente, stable et riche de sens.
Défauts optiques et corrections dioptiques
Dans l’œil idéal, ou œil emmétrope, les rayons parallèles provenant de l’infini se focalisent exactement sur la rétine sans effort accommodatif. Cependant, chez une grande partie de la population, des défauts optiques, ou amétropies, perturbent ce schéma et entraînent une vision floue. Parmi eux, la myopie, l’hypermétropie, l’astigmatisme et la presbytie sont les plus fréquents et représentent un enjeu de santé publique majeur, puisqu’on estime que plus de 50% de la population mondiale sera myope d’ici 2050 selon l’OMS.
La myopie se caractérise par une focalisation des rayons lumineux en avant de la rétine, soit parce que le globe oculaire est trop long, soit parce que la puissance optique de la cornée et du cristallin est excessive. Le sujet voit bien de près mais mal de loin. La correction repose sur des lentilles divergentes (verres ou lentilles de contact) ou sur la chirurgie réfractive cornéenne (LASIK, PRK) qui aplatit la cornée pour réduire sa puissance. À l’inverse, l’hypermétropie correspond à une focalisation en arrière de la rétine, liée à un globe trop court ou à une puissance optique insuffisante ; elle se corrige par des lentilles convergentes.
L’astigmatisme résulte d’une courbure irrégulière de la cornée (ou plus rarement du cristallin), qui se comporte comme un système optique plus puissant dans un méridien que dans un autre. L’image d’un point se projette alors comme une ligne floue, entraînant une vision déformée à toutes les distances. La correction repose sur des lentilles toriques, qui compensent cette asymétrie de courbure. Quant à la presbytie, elle est due à la perte progressive de la capacité d’accommodation liée au durcissement du cristallin avec l’âge, rendant difficile la vision de près à partir de la quarantaine ; elle se corrige par des verres progressifs, des lentilles multifocales ou, dans certains cas, par des techniques de chirurgie réfractive spécifiques.
Vous vous demandez comment choisir entre lunettes, lentilles ou chirurgie pour corriger un défaut de vision ? La décision dépend de plusieurs facteurs : type et importance de l’amétropie, âge, état de la cornée, mode de vie et attentes visuelles. Un bilan ophtalmologique complet, incluant souvent une topographie cornéenne et une mesure précise de la réfraction, permet de déterminer la meilleure stratégie de correction. Dans tous les cas, l’objectif reste le même : rétablir une convergence parfaite des rayons lumineux sur la rétine, en reconstruisant un système optique aussi proche que possible de l’œil emmétrope.
Adaptation pupillaire et régulation de la luminance
L’adaptation pupillaire constitue l’un des mécanismes les plus visibles du fonctionnement optique de l’œil humain. La pupille, ouverture centrale de l’iris, agit comme un diaphragme variable qui régule la quantité de lumière pénétrant dans l’œil. Son diamètre peut varier approximativement de 2 à 8 millimètres, modifiant ainsi par un facteur d’environ 16 la quantité de lumière atteignant la rétine. Cette adaptation est essentielle pour protéger les photorécepteurs d’un excès de lumière et optimiser la vision dans des conditions d’éclairement très diverses.
Le réflexe photomoteur pupillaire est contrôlé par un équilibre entre le système parasympathique (constriction, ou myosis) et le système orthosympathique (dilatation, ou mydriase). En forte luminosité, le muscle sphincter de l’iris se contracte, réduisant le diamètre pupillaire et améliorant la profondeur de champ, à la manière d’un diaphragme fermé sur un objectif photographique. En faible lumière, le muscle dilatateur se contracte, augmentant la taille de la pupille pour laisser entrer davantage de photons et améliorer la sensibilité globale du système visuel.
Au-delà de la simple régulation de lumière, la taille de la pupille influence aussi la qualité optique de l’image. Une pupille trop large accroît l’impact des aberrations sphériques et des défauts de surface cornéenne, réduisant la netteté ; une pupille modérément contractée (autour de 3 mm) tend au contraire à optimiser l’acuité visuelle en limitant ces aberrations, tout en évitant les effets de diffraction observés pour des ouvertures très petites. C’est pourquoi nous voyons souvent plus net en plissant légèrement les yeux : ce geste réduit artificiellement le diamètre pupillaire effectif et améliore la profondeur de champ.
L’adaptation à la luminance ne se limite cependant pas à la seule pupille. Les mécanismes de phototransduction au niveau des photorécepteurs s’ajustent eux aussi, en modulant la sensibilité aux photons via des changements dans la concentration de GMPc, de calcium intracellulaire et dans l’état des pigments visuels. L’ensemble de ces régulations, allant de la microseconde (réflexe pupillaire) à la minute (adaptation rétinienne complète à l’obscurité), permet à l’œil humain de fonctionner sur une plage dynamique d’intensité lumineuse de plus de 109, depuis la nuit sans lune jusqu’au plein soleil. Sans cette formidable capacité d’adaptation, notre expérience visuelle serait soit constamment éblouie, soit plongée dans l’obscurité.