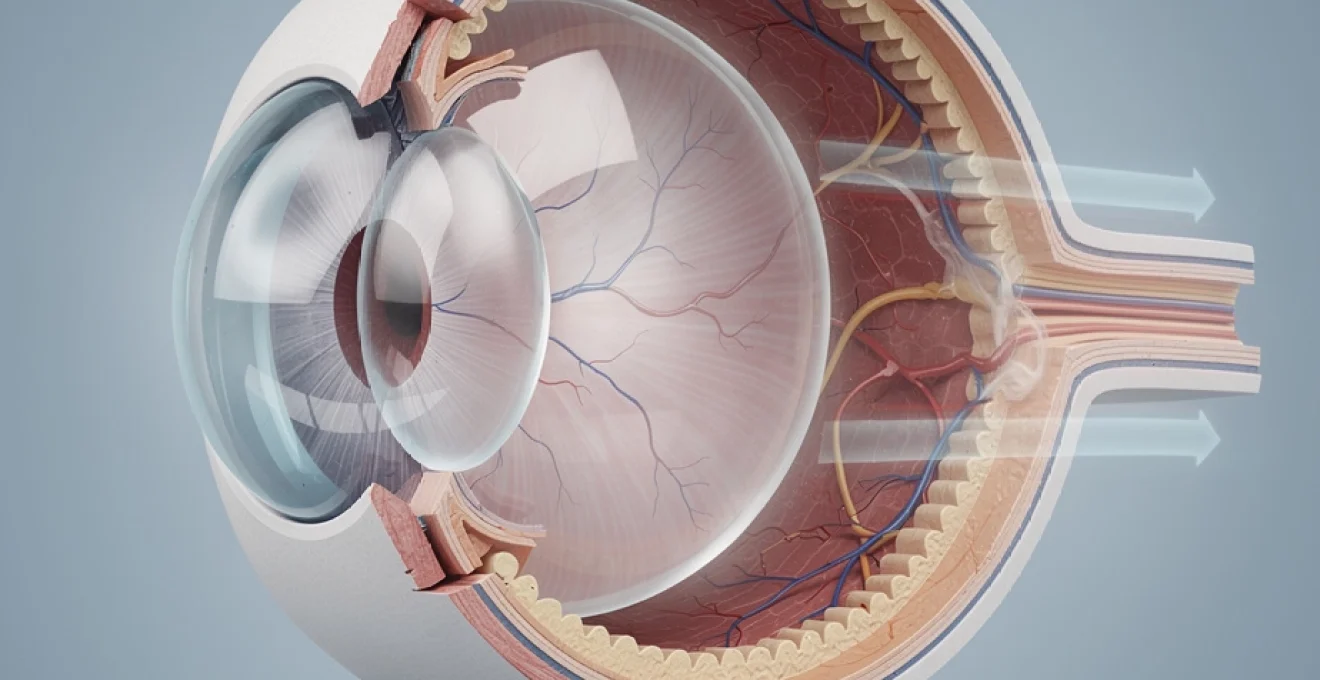
Le globe oculaire représente l’un des organes les plus sophistiqués du corps humain, alliant complexité structurelle et précision fonctionnelle. Mesurant environ 24 millimètres de diamètre pour un poids de seulement 7 grammes, cet organe sensoriel concentre une architecture remarquable qui permet la transformation de la lumière en information visuelle. La protection des éléments internes constitue un défi constant face aux agressions extérieures, nécessitant des mécanismes de défense multicouches perfectionnés au fil de l’évolution. Cette organisation sophistiquée garantit non seulement la survie des structures délicates mais aussi le maintien optimal des fonctions visuelles essentielles à la perception de notre environnement.
Anatomie des tuniques oculaires : sclérotique, choroïde et rétine
L’architecture du globe oculaire repose sur trois tuniques concentriques, chacune ayant des propriétés spécifiques qui contribuent à la protection et au fonctionnement optimal de l’œil. Cette organisation en couches superposées rappelle celle d’un système de sécurité à niveaux multiples, où chaque barrière assume des fonctions protectrices distinctes tout en participant à l’intégrité globale de l’organe.
Structure fibreuse de la sclérotique et résistance mécanique du globe
La sclérotique forme la tunique externe du globe oculaire, constituant une enveloppe fibreuse résistante qui entoure les cinq sixièmes postérieurs de l’œil. Cette membrane, communément appelée « blanc de l’œil », présente une épaisseur variable, atteignant son maximum au niveau du pôle postérieur (environ 1 millimètre) et s’amincissant progressivement vers l’équateur (0,5 millimètre). Sa composition riche en fibres de collagène de type I confère à cette structure une résistance mécanique exceptionnelle, capable de supporter des pressions intraoculaires pouvant atteindre 21 mmHg en conditions normales.
La sclérotique présente de nombreux orifices qui permettent le passage des structures vasculaires et nerveuses essentielles au fonctionnement oculaire. Le foramen scléral postérieur, perforé par les fibres du nerf optique, constitue le point de passage principal vers les centres nerveux. Les orifices antérieurs, moyens et postérieurs assurent respectivement le transit des artères ciliaires antérieures, des veines vortiqueuses et des vaisseaux ciliaires longs et courts. Cette perméabilité sélective illustre parfaitement l’équilibre entre protection et fonctionnalité que doit maintenir cette tunique externe.
Vascularisation choroïdienne et irrigation des photorécepteurs
La choroïde représente la tunique vasculaire de l’œil, concentrant près de 90% du flux sanguin oculaire total. Cette couche intermédiaire assure l’approvisionnement nutritionnel des structures rétiniennes externes, notamment des photorécepteurs dont le métabolisme énergétique est particulièrement élevé. L’organisation anatomique de la choroïde en trois sous-couches distinctes optimise cette fonction nourricière : la couche des gros vaisseaux (couche de Haller), la couche des vaisseaux moyens (couche de Sattler) et la choriocapillaire.
La choriocapillaire mérite une attention particulière car elle forme un réseau capillaire dense situé directement sous l’épithélium pigmentaire rétinien. Ce plexus vasculaire présente des caracté
p>ristiques de perméabilité particulièrement élevées, permettant des échanges rapides d’oxygène, de glucose et de vitamines liposolubles, notamment la vitamine A indispensable au cycle visuel. En retour, les photorécepteurs y déversent leurs déchets métaboliques, qui sont éliminés par la circulation choroïdienne. Ce système d’irrigation en circuit court garantit la survie des cônes et des bâtonnets, dont l’activité ne peut tolérer ni hypoxie ni variations importantes de température. En agissant comme un véritable radiateur biologique, la choroïde contribue aussi à dissiper la chaleur produite par l’absorption massive de photons au niveau de la rétine.
Sur le plan protecteur, la pigmentation intense de la choroïde joue le rôle d’un revêtement anti-reflet, comparable au noir mat à l’intérieur d’un appareil photo. Les mélanocytes absorbent la lumière diffusée et limitent les phénomènes de réflexion interne susceptibles de dégrader la netteté de l’image rétinienne. Cette chambre noire physiologique réduit l’éblouissement et protège indirectement les photorécepteurs d’une exposition excessive à l’énergie lumineuse. Toute atteinte de cette vascularisation, comme dans certaines choroïdopathies ou anomalies de la perfusion, peut rapidement compromettre la fonction visuelle centrale.
Organisation stratifiée de la rétine neurosensorielle
La rétine constitue la tunique nerveuse du globe oculaire, et se distingue par une organisation stratifiée en dix couches successives. Cette architecture complexe permet de transformer un simple flux de photons en influx nerveux hautement codé, interprétable par le cerveau. On y retrouve notamment, de la périphérie vers le nerf optique, les photorécepteurs (cônes et bâtonnets), les cellules bipolaires, horizontales, amacrines, puis les cellules ganglionnaires dont les axones forment le nerf optique. Chacune de ces couches participe à un traitement progressif de l’information, un peu comme les différentes cartes électroniques d’un appareil de haute précision qui affinent successivement le signal.
L’équilibre entre cônes et bâtonnets illustre bien l’adaptation fonctionnelle de la rétine. Les cônes, concentrés dans la macula et surtout la fovéa, assurent la vision fine et la perception des couleurs, indispensables à la lecture ou à la reconnaissance des visages. Les bâtonnets, beaucoup plus nombreux en périphérie, sont spécialisés dans la vision scotopique (en faible luminosité) et la détection des mouvements dans le champ visuel. Cette répartition spatiale optimise la couverture du champ visuel tout en préservant la précision centrale. D’un point de vue protecteur, la rétine bénéficie aussi de mécanismes de maintenance permanents, comme le renouvellement continu des disques photorécepteurs par l’épithélium pigmentaire rétinien (EPR), limitant l’accumulation de toxines photo-oxydatives.
L’EPR, situé entre la rétine neurosensorielle et la choroïde, joue un rôle clé à l’interface entre vision et protection. Ses cellules pigmentées absorbent la lumière parasite, phagocytent les segments externes usés des photorécepteurs et participent à la régénération des pigments visuels. Elles forment également une barrière hémato-rétinienne externe grâce à leurs jonctions serrées, empêchant protéines et toxines d’origine choroïdienne de diffuser librement vers la neurorétine. En cas de rupture de cette cohésion, comme lors d’un décollement de rétine, l’espace sous-rétinien se remplit de liquide, privant brutalement les photorécepteurs de leur soutien métabolique.
Jonction scléro-cornéenne et maintien de la pression intraoculaire
Au niveau antérieur du globe, la jonction entre la sclérotique et la cornée forme le limbe scléro-cornéen, zone stratégique pour la stabilité mécanique et hydraulique de l’œil. Cette région en anneau abrite le sillon scléral interne, dans lequel se situe le canal de Schlemm, véritable collecteur veineux de l’humeur aqueuse. Sur le plan structurel, le limbe associe des fibres collagéniques sclérales épaisses à une transition progressive vers le stroma cornéen plus organisé, ce qui lui confère une capacité à absorber les contraintes sans se déformer de façon permanente. Il joue alors le rôle de charnière rigide mais fonctionnelle entre la coque fibreuse opaque et le hublot transparent.
Sur le plan hydrodynamique, l’angle irido-cornéen, localisé précisément au niveau du limbe, contient le réseau trabéculaire par lequel s’effectue le drainage de l’humeur aqueuse. Le bon fonctionnement de cette micro-architecture conditionne le maintien d’une pression intraoculaire stable, généralement comprise entre 10 et 21 mmHg. Une évacuation insuffisante entraîne une élévation progressive de cette pression, avec un risque de compression des fibres du nerf optique au niveau de la papille. À l’inverse, une pression trop basse compromet la rigidité du globe et expose aux déformations mécaniques, notamment lors de traumatismes. Vous le voyez, cette zone d’apparence anodine se révèle en réalité capitale pour la protection à long terme des éléments internes.
Chambres oculaires et circulation de l’humeur aqueuse
Au sein du segment antérieur de l’œil, deux cavités remplies de liquide, la chambre antérieure et la chambre postérieure, assurent une circulation continue d’humeur aqueuse. Cette circulation joue un rôle crucial dans la transparence des milieux, la nutrition des structures avasculaires comme la cornée et le cristallin, ainsi que dans le maintien de la pression intraoculaire. On peut comparer ce système à un circuit de climatisation miniaturisé, où production, circulation et évacuation du fluide doivent rester finement équilibrées pour garantir un climat interne stable.
Production ciliaire et composition biochimique de l’humeur aqueuse
L’humeur aqueuse est produite par les procès ciliaires du corps ciliaire, situés en arrière de l’iris, dans la chambre postérieure. Cette production combine diffusion passive, ultrafiltration et sécrétion active de solutés via des pompes ioniques, notamment la Na⁺/K⁺-ATPase et des co-transporteurs bicarbonate. Le débit moyen de sécrétion est estimé entre 2 et 3 microlitres par minute chez l’adulte, avec des variations diurnes. Après sa production, l’humeur aqueuse traverse la pupille pour rejoindre la chambre antérieure, avant d’être évacuée vers le canal de Schlemm.
Sur le plan biochimique, l’humeur aqueuse est un ultrafiltrat du plasma, pauvre en protéines (environ 1 % de la concentration plasmatique) mais riche en nutriments indispensables : glucose, acide ascorbique (vitamine C), électrolytes, acides aminés. Cette composition spécifique protège la transparence de la cornée et du cristallin en limitant la diffusion de macromolécules potentiellement opacifiantes. La forte concentration en vitamine C, jusqu’à 20 à 30 fois celle du plasma, joue également un rôle essentiel d’antioxydant intraoculaire, neutralisant les radicaux libres générés par l’exposition chronique à la lumière. Sans cette protection biochimique, les dommages oxydatifs sur le cristallin et la cornée seraient beaucoup plus fréquents.
Drainage trabéculaire et régulation de la pression intraoculaire
Le principal mécanisme de drainage de l’humeur aqueuse est le système trabéculo-canalaire, localisé dans l’angle irido-cornéen. L’humeur aqueuse s’infiltre d’abord à travers le trabéculum, réseau de fines lamelles collagéniques et de cellules endothéliales disposées en éventail. Elle gagne ensuite le canal de Schlemm, puis un réseau de veines épisclérales qui la renvoient vers la circulation systémique. Ce circuit de sortie fonctionne comme un filtre à plusieurs étages, contrôlant à la fois le débit d’évacuation et la résistance à l’écoulement. C’est précisément cette résistance qui, en lien avec le débit de production, détermine le niveau de pression intraoculaire.
Un second mécanisme de drainage, dit voie uvéosclérale, permet à une fraction de l’humeur aqueuse de quitter la chambre antérieure en traversant l’iris, le corps ciliaire et la choroïde, avant d’être résorbée dans la sclère. Bien que cette voie soit minoritaire (10 à 20 % du drainage total selon les études), elle représente un relais important, notamment en cas de dysfonction du trabéculum. Les thérapeutiques modernes du glaucome exploitent d’ailleurs ces deux voies : certains collyres abaissent la production ciliaire, d’autres augmentent l’élimination trabéculaire ou uvéosclérale. Pour préserver vos nerfs optiques, la régulation de cette micro-hydraulique reste donc un enjeu majeur, particulièrement après 40 ans.
Barrières hémato-aqueuses et protection contre les toxines
Pour que l’humeur aqueuse puisse protéger les éléments internes sans les exposer à des substances potentiellement nocives, l’œil dispose de barrières hémato-aqueuses strictes. La première est assurée par les jonctions serrées des cellules endothéliales des capillaires du corps ciliaire, qui limitent le passage des protéines plasmatiques et des molécules de grande taille. La seconde réside dans l’épithélium non pigmenté des procès ciliaires, dont les jonctions serrées contrôlent la composition finale de l’humeur aqueuse sécrétée vers les chambres oculaires. Ce double filtre fonctionne comme une station de traitement d’eau à haute sécurité, sélectionnant avec rigueur les éléments autorisés à pénétrer dans le segment antérieur.
Ces barrières ont aussi une dimension immunologique. En maintenant une très faible teneur en protéines et en cellules immunitaires, elles contribuent à un environnement relativement immunoprivilégié, réduisant le risque de réaction inflammatoire incontrôlée au niveau de la cornée et du cristallin. Toutefois, cette protection a son revers : en cas d’infection intraoculaire ou d’uvéite, l’accès des cellules immunitaires et des antibiotiques peut être limité, compliquant la prise en charge thérapeutique. Lorsque la barrière hémato-aqueuse est rompue, par exemple lors d’une inflammation importante, l’humeur aqueuse se charge de protéines, provoquant un tyndall visible à la lampe à fente, signe clinique d’une atteinte de l’intégrité protectrice intraoculaire.
Pathophysiologie du glaucome par angle fermé
Le glaucome par angle fermé illustre de manière dramatique ce qui se produit lorsque la circulation de l’humeur aqueuse est brutalement interrompue. Dans cette forme de glaucome, l’angle irido-cornéen se ferme mécaniquement, empêchant l’humeur aqueuse d’atteindre le trabéculum et le canal de Schlemm. La cause la plus fréquente est une pupille en semi-mydriase, où l’iris vient se coller contre le cristallin, créant un bloc pupillaire. La pression augmente alors dans la chambre postérieure, poussant la racine de l’iris vers l’avant et obstruant l’angle. Ce cercle vicieux aboutit en quelques heures à une élévation majeure de la pression intraoculaire, parfois au-delà de 50-60 mmHg.
Cliniquement, le patient présente un œil rouge, extrêmement douloureux, une baisse rapide de la vision, des céphalées, des nausées et parfois des vomissements. La cornée apparaît œdémateuse, rendant la pupille difficile à examiner. Sans intervention rapide (collyres, médicaments par voie générale, puis iridotomie laser pour recréer un passage de l’humeur aqueuse), les fibres du nerf optique sont compromises de façon irréversible. Ce tableau aigu illustre à quel point l’intégrité anatomique de l’angle irido-cornéen est essentielle pour la protection des éléments internes. Si vous présentez des antécédents familiaux de glaucome ou une hypermétropie forte, un contrôle régulier de la profondeur de votre chambre antérieure peut permettre de prévenir ce type d’épisode.
Cristallin et mécanismes d’accommodation visuelle
Le cristallin est une lentille biconvexe transparente, suspendue en arrière de l’iris par la zonule de Zinn, elle-même ancrée au corps ciliaire. Son pouvoir réfractif d’environ 20 à 22 dioptries complète celui de la cornée pour focaliser les rayons lumineux sur la rétine. Sa particularité réside dans sa capacité à modifier sa courbure grâce au muscle ciliaire, permettant l’accommodation, c’est-à-dire l’ajustement de la mise au point entre vision de loin et de près. On peut le comparer à un objectif à focale variable, dont la géométrie se modifie en temps réel pour garder l’image nette sur le capteur rétinien.
Lorsque vous regardez au loin, le muscle ciliaire est relâché, la zonule est tendue, et le cristallin adopte une forme plus plate, adaptée aux faibles convergences. À l’inverse, pour lire un texte rapproché, le muscle ciliaire se contracte, diminue la tension des fibres zonulaires et permet au cristallin de se bomber, augmentant ainsi son pouvoir de convergence. Ce mécanisme est particulièrement performant chez l’enfant et l’adulte jeune, chez qui l’amplitude d’accommodation peut dépasser 10 dioptries. Avec l’âge, le cristallin se sclérose, perd de son élasticité et sa capacité à se déformer diminue : c’est la presbytie, qui oblige progressivement à éloigner le texte puis à recourir à des verres de près.
Sur le plan protecteur, le cristallin joue également un rôle de filtre optique. Il absorbe une partie significative des rayons UV et de la lumière bleue, réduisant l’exposition directe de la rétine aux longueurs d’onde les plus énergétiques. Toutefois, cette fonction de bouclier a un coût : au fil du temps, les protéines cristalliniennes subissent des altérations oxydatives, s’agrègent et perdent leur transparence, aboutissant à la cataracte. Cette opacification progressive, qui reste aujourd’hui la première cause de cécité réversible dans le monde, illustre la limite naturelle des mécanismes de protection internes. L’intervention chirurgicale moderne (phacoémulsification) remplace alors le cristallin opacifié par un implant artificiel, restituant la transparence et parfois corrigeant simultanément les défauts de réfraction.
Corps vitré et maintien architectural du segment postérieur
Le corps vitré occupe environ les quatre cinquièmes du volume du globe oculaire et remplit le segment postérieur, entre le cristallin et la rétine. Ce gel transparent, composé à 98-99 % d’eau, d’un réseau de collagène et d’acide hyaluronique, agit comme un remplissage structurel qui maintient la forme du globe et plaque la rétine contre l’épithélium pigmentaire. À la différence de l’humeur aqueuse, son renouvellement est extrêmement lent, ce qui en fait un milieu relativement stable mais vulnérable aux accumulations progressives de débris.
Composition collagénique et propriétés viscoélastiques du vitré
La matrice vitréenne repose sur un réseau lâche de fibrilles de collagène de type II, associé à d’autres types de collagène (IX, V/XI) et à des protéoglycanes, principalement l’acide hyaluronique. Cette combinaison confère au vitré des propriétés viscoélastiques remarquables : il résiste aux déformations rapides, amortit les chocs et revient à sa forme initiale, un peu comme un coussin de gel absorbant les vibrations. Cette élasticité protège la rétine des variations soudaines de pression ou d’accélération, par exemple lors de mouvements brusques de la tête ou d’impacts modérés.
Avec l’âge, l’équilibre entre la phase gélifiée et la phase liquide du vitré se modifie : le gel se liquéfie partiellement (synérèse vitréenne), les fibrilles de collagène se réorganisent et peuvent former des condensations visibles sous forme de corps flottants (myodésopsies). Si ces phénomènes restent physiologiques dans la majorité des cas, ils traduisent néanmoins une perte progressive des propriétés mécaniques optimales. Cette dégradation peut favoriser, à terme, la survenue de tractions anormales sur la rétine, notamment lors du décollement postérieur du vitré, processus presque universel après 60 ans.
Interface vitréo-rétinienne et prévention du décollement rétinien
L’interface vitréo-rétinienne correspond aux zones d’adhérence entre la hyaloïde postérieure (membrane périphérique du vitré) et la surface interne de la rétine. Ces adhérences sont particulièrement fortes au niveau de la papille, de la macula, de l’ora serrata et autour des vaisseaux rétiniens. Tant que ces attaches restent équilibrées, le vitré exerce une traction homogène qui contribue à maintenir la rétine plaquée contre la choroïde. On peut assimiler ce système à une fine pellicule adhésive maintenant un poster bien tendu contre un mur : tant que la colle est uniformément répartie, le support reste parfaitement appliqué.
Lorsque le vitré se liquéfie et que la hyaloïde postérieure se détache partiellement, des tractions focales peuvent s’exercer sur certaines zones de la rétine, en particulier si des adhérences pathologiques existent (zones de dégénérescence lattice, cicatrices, foyers inflammatoires). Ces tractions peuvent provoquer des déchirures rétiniennes, porte d’entrée au décollement de rétine rhegmatogène. Dans ce cas, le liquide vitréen s’infiltre progressivement sous la rétine neurosensorielle et la sépare de l’épithélium pigmentaire, privant les photorécepteurs de leur soutien métabolique. Les symptômes d’alerte – éclairs lumineux, augmentation brutale des corps flottants, voile noir dans le champ visuel – doivent conduire à une consultation urgente. Une prise en charge précoce (photocoagulation laser, chirurgie vitréo-rétinienne) reste la clé pour préserver la fonction visuelle.
Métabolisme vitréen et élimination des déchets cellulaires
Bien que peu vascularisé (la vascularisation hyaloïde disparaît peu après la naissance), le vitré participe au métabolisme intraoculaire en servant de réservoir diffusif pour l’oxygène et certains nutriments issus de la rétine et du corps ciliaire. Il facilite aussi, à faible échelle, le transport de métabolites et de déchets cellulaires vers les structures voisines capables de les éliminer, notamment la rétine et la choroïde. Ce rôle reste plus discret que celui de l’humeur aqueuse, mais contribue malgré tout à l’homéostasie globale du segment postérieur.
Par ailleurs, le vitré possède des mécanismes de défense antioxydante et enzymatique, incluant des enzymes comme la superoxyde dismutase et la catalase. Ils limitent l’accumulation de produits de glycation avancée et d’agrégats protéiques susceptibles de troubler la transparence du gel. Lorsque ces mécanismes sont dépassés, comme dans certains contextes métaboliques (diabète mal équilibré, stress oxydatif chronique), le vitré peut devenir le siège de condensations, d’hémorragies ou d’opacités durables. Dans les formes sévères – hémorragies intravitréennes d’origine diabétique par exemple – seule une vitrectomie (ablation chirurgicale du vitré) permet de restaurer un environnement optique compatible avec une bonne transmission lumineuse.
Barrières protectrices et défenses immunologiques oculaires
Au-delà de sa structure mécanique, le globe oculaire s’appuie sur un ensemble de barrières protectrices et de mécanismes de défense immunologique pour préserver ses éléments internes. La première ligne de défense est constituée par les paupières, la conjonctive et le film lacrymal, qui protègent la surface oculaire contre les corps étrangers, les agents infectieux et la dessiccation. Les larmes, riches en lysozyme, lactoferrine, immunoglobulines A sécrétoires et facteurs de croissance, forment un véritable bouclier antimicrobien tout en assurant la lubrification indispensable de la cornée.
En profondeur, deux grandes barrières limitent les échanges incontrôlés entre le sang et les tissus oculaires : la barrière hémato-aqueuse et la barrière hémato-rétinienne. Cette dernière comprend une composante interne (jonctions serrées des cellules endothéliales des capillaires rétiniens) et une composante externe (jonctions serrées de l’épithélium pigmentaire rétinien). Ensemble, elles restreignent l’accès des agents pathogènes, des toxines et même de nombreuses molécules médicamenteuses aux structures neurosensorielles. C’est en partie grâce à elles que la rétine bénéficie d’un statut d’organe immunoprivilégié, limitant les réactions inflammatoires susceptibles de compromettre irréversiblement la vision.
Cependant, cet isolement relatif ne signifie pas absence d’immunité. L’œil dispose de cellules présentatrices d’antigènes, de microglies rétiniennes et d’un réseau complexe de cytokines régulatrices qui orchestrent des réponses immunitaires mesurées. En cas d’agression – infection, traumatisme, chirurgie – ces mécanismes se mobilisent pour contenir l’atteinte tout en minimisant les dommages collatéraux. Dans certains contextes, cet équilibre peut se rompre et conduire à des uvéites auto-immunes ou à des réactions inflammatoires prolongées, dont les conséquences sur la transparence des milieux (synéchies, opacités vitréennes, œdème maculaire) rappellent à quel point la préservation de la clarté et de l’homéostasie interne est cruciale.
Comprendre ces multiples barrières – mécaniques, optiques, biochimiques et immunologiques – permet de mieux appréhender pourquoi un simple traumatisme, une infection mal traitée ou une élévation silencieuse de la pression intraoculaire peuvent avoir des répercussions majeures sur la vision. En pratique, la meilleure façon de profiter durablement de cette architecture d’exception reste la prévention : protéger ses yeux des UV, éviter les traumatismes, contrôler ses facteurs de risque vasculaires et consulter régulièrement un ophtalmologiste, surtout après 40 ans ou en cas de symptômes visuels inhabituels.